Η ηλεκτρονιακή δομή και ο περιοδικός πίνακας είναι από τα... Δες περισσότερα
Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟΕίναι δωρεάν!
Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Knowunity AI
Περισσότερα
Μαθήματα
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Δείξε όλα τα θέματα
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Δείξε όλα τα θέματα
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Δείξε όλα τα θέματα
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Δείξε όλα τα θέματα
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Δείξε όλα τα θέματα
1,026
•
Ενημερώθηκε Apr 27, 2026
•
Electra Athanasopoulou
@electrrrv
Η ηλεκτρονιακή δομή και ο περιοδικός πίνακας είναι από τα... Δες περισσότερα

















Η θεωρία του Bohr επανάστασε τον τρόπο που βλέπουμε τα άτομα. Σύμφωνα με την 1η συνθήκη του, τα ηλεκτρόνια δεν κινούνται όπου θέλουν, αλλά μόνο σε συγκεκριμένες τροχιές με καθορισμένη ενέργεια.
Το μυστικό είναι ότι η ενέργεια είναι κβαντισμένη - δηλαδή παίρνει μόνο συγκεκριμένες τιμές, όπως τα χρήματα που μπορείς να έχεις μόνο σε πολλαπλάσια των 5 λεπτών. Η ενέργεια ενός ηλεκτρονίου δίνεται από τον τύπο E = -2,18·10⁻¹⁸/n² J.
Το αρνητικό πρόσημο σημαίνει ότι πρέπει να δώσεις ενέργεια για να "κλέψεις" ένα ηλεκτρόνιο από το άτομο. Όταν ένα ηλεκτρόνιο απορροφά ενέργεια, πηγαίνει σε υψηλότερη στιβάδα (διεγερμένη κατάσταση), αλλά γρήγορα επιστρέφει εκπέμποντας φωτόνια με συγκεκριμένη ενέργεια.
💡 Θυμήσου: Στη θεμελιώδη κατάσταση, όλα τα ηλεκτρόνια βρίσκονται όσο πιο κοντά στον πυρήνα γίνεται - εκεί έχουν τη μικρότερη ενέργεια!

Όταν ένα ηλεκτρόνιο "πέφτει" από υψηλότερη σε χαμηλότερη στιβάδα, εκπέμπει φωτόνιο με ενέργεια ΔΕ = Eτελική - Eαρχική. Αυτή η ενέργεια μετατρέπεται σε φως με συχνότητα f = ΔΕ/h, όπου h είναι η σταθερά του Planck (6,63·10⁻³⁴ J·s).
Για παράδειγμα, στη μετάπτωση από n=4 σε n=1, το ηλεκτρόνιο εκπέμπει περισσότερη ενέργεια από ό,τι στη μετάπτωση n=3 σε n=2. Αυτό σημαίνει ότι το πρώτο φωτόνιο έχει μικρότερο μήκος κύματος (λ₁ < λ₂).
Όταν θερμαίνουμε μια αέρια ουσία, παράγεται γραμμικό φάσμα με συγκεκριμένες γραμμές. Αντίθετα, οι στερεές και υγρές ουσίες δίνουν συνεχές φάσμα. Κάθε στοιχείο έχει το δικό του μοναδικό φάσμα - σαν δακτυλικό αποτύπωμα!
💡 Προσοχή: Για να διεγερθούν όλα τα άτομα σε ένα δείγμα, χρειάζονται τόσα φωτόνια όσα και τα άτομα (χρησιμοποίησε τον αριθμό Avogadro)!

Η θεωρία του Bohr λειτουργούσε μόνο για μονοηλεκτρονιακά άτομα (H, He⁺, Li²⁺) και δεν εξηγούσε τα πολυηλεκτρονιακά άτομα. Έτσι, οι επιστήμονες ανέπτυξαν νέες θεωρίες που άλλαξαν τελείως την εικόνα μας για τα άτομα.
Ο De Broglie πρότεινε ότι τα μικρά σωματίδια έχουν διττή φύση - είναι και σωματίδια και κύματα. Ένα ηλεκτρόνιο που κινείται γρήγορα συμπεριφέρεται σαν κύμα με μήκος κύματος λ = h/mv.
Ο Heisenberg διατύπωσε την αρχή της αβεβαιότητας: δεν μπορούμε να γνωρίζουμε ταυτόχρονα με ακρίβεια τη θέση και την ταχύτητα ενός ηλεκτρονίου. Αυτό δεν είναι τεχνικό πρόβλημα - είναι θεμελιώδης νόμος της φύσης!
Όλες αυτές οι ιδέες οδήγησαν στην εξίσωση του Schrödinger και στην έννοια των ατομικών τροχιακών - χώρων όπου έχουμε πιθανότητα να βρούμε ένα ηλεκτρόνιο.
💡 Βασική διαφορά: Δεν μιλάμε πλέον για συγκεκριμένες τροχιές, αλλά για περιοχές πιθανότητας!

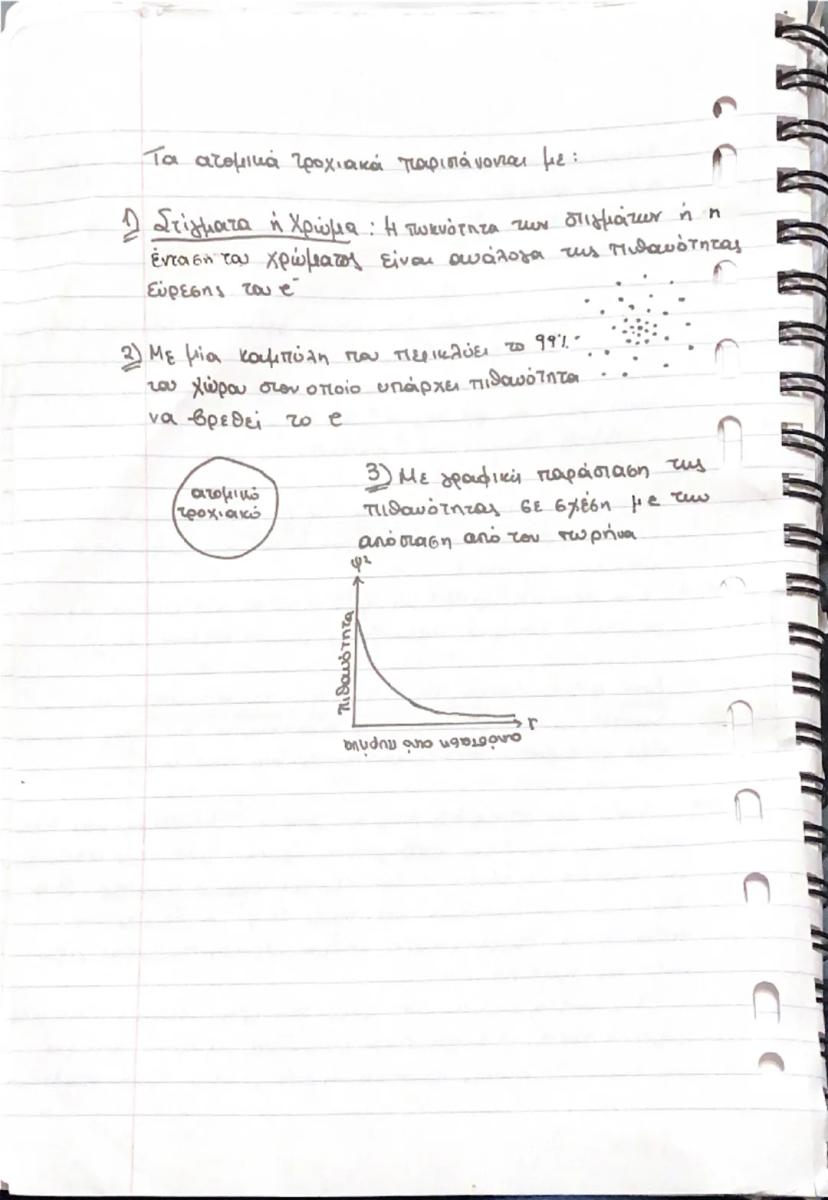
Τα ατομικά τροχιακά είναι οι τρισδιάστατοι χώροι όπου έχουμε 99% πιθανότητα να βρούμε ένα ηλεκτρόνιο. Κάθε τροχιακό έχει τρία χαρακτηριστικά: μέγεθος, σχήμα και προσανατολισμό στο χώρο.
Μπορούμε να παραστήσουμε τα τροχιακά με τρεις τρόπους: με στίγματα (όσο πιο πυκνά, τόσο μεγαλύτερη η πιθανότητα), με καμπύλες που περικλείουν το 99% της πιθανότητας, ή με γραφικές παραστάσεις που δείχνουν πώς αλλάζει η πιθανότητα με την απόσταση από τον πυρήνα.
Η κυματοσυνάρτηση ψ από μόνη της δεν έχει φυσικό νόημα, αλλά το ψ² μας δίνει την πιθανότητα εύρεσης του ηλεκτρονίου σε κάθε σημείο. Αυτή είναι η βάση για να κατανοήσουμε τη δομή των ατόμων!
💡 Σημαντικό: Το τροχιακό δεν είναι η διαδρομή του ηλεκτρονίου, αλλά ο χώρος όπου πιθανότατα θα το βρούμε!

Κάθε ηλεκτρόνιο στο άτομο έχει μια μοναδική "διεύθυνση" που καθορίζεται από τέσσερις κβαντικούς αριθμούς. Είναι σαν το ταχυδρομικό κώδικα που καθορίζει ακριβώς πού βρίσκεται!
Ο κύριος κβαντικός αριθμός n (1,2,3...) δείχνει την απόσταση από τον πυρήνα και καθορίζει τη στιβάδα (K, L, M, N...). Όσο μεγαλύτερο το n, τόσο μεγαλύτερη η ενέργεια.
Ο αζιμουθιακός αριθμός l καθορίζει το σχήμα του τροχιακού: l=0→s (σφαιρικό), l=1→p (αλτήρας), l=2→d (πολύπλοκα σχήματα), l=3→f (ακόμα πιο πολύπλοκα). Το ζεύγος (n,l) καθορίζει την υποστιβάδα.
Ο μαγνητικός αριθμός ml δείχνει τον προσανατολισμό του τροχιακού. Ο spin ms (±½) δείχνει την "αυτοπεριστροφή" του ηλεκτρονίου.
💡 Θυμήσου: Η τετράδα (n,l,ml,ms) είναι μοναδική για κάθε ηλεκτρόνιο - δεν μπορούν δύο ηλεκτρόνια να έχουν την ίδια!

Τα s τροχιακά έχουν σφαιρική συμμετρία και η μέγιστη πιθανότητα εύρεσης ηλεκτρονίου είναι πάνω στον πυρήνα. Σε κάθε στιβάδα υπάρχει μόνο ένα s τροχιακό που χωράει 2 ηλεκτρόνια.
Τα p τροχιακά έχουν σχήμα αλτήρα και τρεις προσανατολισμούς (px, py, pz). Έχουν κομβική επιφάνεια - μια περιοχή όπου η πιθανότητα εύρεσης ηλεκτρονίου είναι μηδέν. Συνολικά χωράνε 6 ηλεκτρόνια (3 τροχιακά × 2 ηλεκτρόνια).
Τα d τροχιακά είναι 5 και χωράνε 10 ηλεκτρόνια, ενώ τα f τροχιακά είναι 7 και χωράνε 14 ηλεκτρόνια. Όσο αυξάνεται το l, τόσο πιο περίπλοκα γίνονται τα σχήματα.
Βασική διαφορά: στα s τροχιακά το ηλεκτρόνιο μπορεί να βρεθεί πάνω στον πυρήνα, ενώ στα p η πιθανότητα εκεί είναι μηδέν!
💡 Μνημονικό: s=1 τροχιακό, p=3 τροχιακά, d=5 τροχιακά, f=7 τροχιακά. Πολλαπλάσιασε επί 2 για τα ηλεκτρόνια!

Για να φτιάξεις τη σωστή ηλεκτρονιακή δομή ενός ατόμου, πρέπει να ακολουθήσεις τρεις βασικούς κανόνες που είναι σαν τους κανόνες ενός παιχνιδιού.
Η απαγορευτική αρχή του Pauli λέει ότι σε κάθε τροχιακό χωράνε μέχρι 2 ηλεκτρόνια με αντίθετο spin. Δεν μπορούν δύο ηλεκτρόνια να έχουν την ίδια τετράδα κβαντικών αριθμών.
Η αρχή ελάχιστης ενέργειας λέει ότι τα ηλεκτρόνια μπαίνουν πρώτα στα τροχιακά με τη μικρότερη ενέργεια. Η σειρά είναι: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d... Χρησιμοποίησε το άθροισμα για να θυμάσαι τη σειρά!
Προσοχή: όταν γράφεις κατιόντα, τα ηλεκτρόνια φεύγουν από την υποστιβάδα που γράφεται τελευταία (οριζόντια σειρά), όχι από αυτή που έχει τη μεγαλύτερη ενέργεια!
💡 Μνημονικός κανόνας: Χρησιμοποίησε το διάγραμμα με τις λοξές γραμμές για να θυμάσαι τη σειρά πλήρωσης!

Ο κανόνας του Hund είναι σαν να μοιράζεις καρέκλες σε μια αίθουσα: πρώτα κάθεται από ένας σε κάθε καρέκλα, μετά μπαίνει ο δεύτερος! Τα ηλεκτρόνια τοποθετούνται με παράλληλα spin σε τροχιακά ίδιας ενέργειας.
Στην πράξη: βάζεις πρώτα από ένα ηλεκτρόνιο (με θετικό spin) σε κάθε p, d ή f τροχιακό, και μετά συμπληρώνεις με το δεύτερο (αρνητικό spin).
Για παράδειγμα: C : 1s², 2s², 2p² → p: ↑ ↑ _ N : 1s², 2s², 2p³ → p: ↑ ↑ ↑ O : 1s², 2s², 2p⁴ → p: ↑↓ ↑ ↑
Για να γράψεις την πλήρη τετράδα κβαντικών αριθμών, ξεκινάς από το τελευταίο ηλεκτρόνιο. Η εξώτερη στιβάδα είναι αυτή με το μεγαλύτερο n και καθορίζει τις χημικές ιδιότητες!
💡 Tip: Ο κανόνας Hund εξηγεί γιατί ο άνθρακας έχει 2 μη ζευγαρωμένα ηλεκτρόνια και μπορεί να σχηματίσει 4 δεσμούς!

Ο περιοδικός πίνακας είναι η πιο έξυπνη εφεύρεση της χημείας! Τα 118 γνωστά στοιχεία είναι τοποθετημένα κατά αύξοντα ατομικό αριθμό, έτσι ώστε στοιχεία με παρόμοιες ιδιότητες να βρίσκονται στην ίδια στήλη.
Ο νόμος της περιοδικότητας λέει ότι οι ιδιότητες των στοιχείων επαναλαμβάνονται περιοδικά. Έχει 18 στήλες (ομάδες) και 7 σειρές (περιόδους). Οι σημαντικότερες ομάδες έχουν ονόματα: αλκάλια (IA), αλκαλικές γαίες (IIA), αλογόνα (VIIA), ευγενή αέρια (VIIIA).
Όλα τα ευγενή αέρια (εκτός το He) έχουν δομή ns²np⁶ - αυτό εξηγεί την σταθερότητά τους. Ο πίνακας χωρίζεται σε τομείς s, p, d, f ανάλογα με το πού μπαίνει το τελευταίο ηλεκτρόνιο.
Τομέας s: ομάδες IA-IIA (δομή ns¹ και ns²), Τομέας p: ομάδες IIIA-VIIIA (δομή ns²np¹⁻⁶), Τομέας d: μεταβατικά στοιχεία .
💡 Σημαντικό: Το He ανήκει στον τομέα s, παρότι βρίσκεται στην VIIIA ομάδα!

Για να βρεις τη θέση οποιουδήποτε στοιχείου, χρειάζεσαι μόνο την ηλεκτρονιακή του δομή! Είναι πιο εύκολο απ' ό,τι φαίνεται.
Το μέγιστο n δείχνει τον αριθμό της περιόδου. Για τους τομείς s και p, ο αριθμός ηλεκτρονίων της εξώτερης στιβάδας δίνει τον αριθμό της ομάδας (λατινικό σύστημα).
Για τον τομέα d: το μέγιστο n δίνει την περίοδο, ενώ ο αριθμός της ομάδας = ηλεκτρόνια σε ns + ηλεκτρόνια σε d.
Παράδειγμα: Te → 1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁴
Ο τομέας f περιλαμβάνει τις λανθανίδες (6η περίοδος) και ακτινίδες (7η περίοδος) - τα στοιχεία του παραρτήματος.
💡 Πρακτικό tip: Μάθε πρώτα να γράφεις δομές με βάση το προηγούμενο ευγενές αέριο - είναι πιο σύντομο!








Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
App Store
Google Play
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Electra Athanasopoulou
@electrrrv
Η ηλεκτρονιακή δομή και ο περιοδικός πίνακας είναι από τα πιο σημαντικά κεφάλαια της χημείας που θα σε βοηθήσουν να καταλάβεις πώς συμπεριφέρονται τα άτομα. Μάθε πώς τα ηλεκτρόνια "κινούνται" γύρω από τον πυρήνα και πώς αυτό καθορίζει τις ιδιότητες... Δες περισσότερα

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Η θεωρία του Bohr επανάστασε τον τρόπο που βλέπουμε τα άτομα. Σύμφωνα με την 1η συνθήκη του, τα ηλεκτρόνια δεν κινούνται όπου θέλουν, αλλά μόνο σε συγκεκριμένες τροχιές με καθορισμένη ενέργεια.
Το μυστικό είναι ότι η ενέργεια είναι κβαντισμένη - δηλαδή παίρνει μόνο συγκεκριμένες τιμές, όπως τα χρήματα που μπορείς να έχεις μόνο σε πολλαπλάσια των 5 λεπτών. Η ενέργεια ενός ηλεκτρονίου δίνεται από τον τύπο E = -2,18·10⁻¹⁸/n² J.
Το αρνητικό πρόσημο σημαίνει ότι πρέπει να δώσεις ενέργεια για να "κλέψεις" ένα ηλεκτρόνιο από το άτομο. Όταν ένα ηλεκτρόνιο απορροφά ενέργεια, πηγαίνει σε υψηλότερη στιβάδα (διεγερμένη κατάσταση), αλλά γρήγορα επιστρέφει εκπέμποντας φωτόνια με συγκεκριμένη ενέργεια.
💡 Θυμήσου: Στη θεμελιώδη κατάσταση, όλα τα ηλεκτρόνια βρίσκονται όσο πιο κοντά στον πυρήνα γίνεται - εκεί έχουν τη μικρότερη ενέργεια!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Όταν ένα ηλεκτρόνιο "πέφτει" από υψηλότερη σε χαμηλότερη στιβάδα, εκπέμπει φωτόνιο με ενέργεια ΔΕ = Eτελική - Eαρχική. Αυτή η ενέργεια μετατρέπεται σε φως με συχνότητα f = ΔΕ/h, όπου h είναι η σταθερά του Planck (6,63·10⁻³⁴ J·s).
Για παράδειγμα, στη μετάπτωση από n=4 σε n=1, το ηλεκτρόνιο εκπέμπει περισσότερη ενέργεια από ό,τι στη μετάπτωση n=3 σε n=2. Αυτό σημαίνει ότι το πρώτο φωτόνιο έχει μικρότερο μήκος κύματος (λ₁ < λ₂).
Όταν θερμαίνουμε μια αέρια ουσία, παράγεται γραμμικό φάσμα με συγκεκριμένες γραμμές. Αντίθετα, οι στερεές και υγρές ουσίες δίνουν συνεχές φάσμα. Κάθε στοιχείο έχει το δικό του μοναδικό φάσμα - σαν δακτυλικό αποτύπωμα!
💡 Προσοχή: Για να διεγερθούν όλα τα άτομα σε ένα δείγμα, χρειάζονται τόσα φωτόνια όσα και τα άτομα (χρησιμοποίησε τον αριθμό Avogadro)!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Η θεωρία του Bohr λειτουργούσε μόνο για μονοηλεκτρονιακά άτομα (H, He⁺, Li²⁺) και δεν εξηγούσε τα πολυηλεκτρονιακά άτομα. Έτσι, οι επιστήμονες ανέπτυξαν νέες θεωρίες που άλλαξαν τελείως την εικόνα μας για τα άτομα.
Ο De Broglie πρότεινε ότι τα μικρά σωματίδια έχουν διττή φύση - είναι και σωματίδια και κύματα. Ένα ηλεκτρόνιο που κινείται γρήγορα συμπεριφέρεται σαν κύμα με μήκος κύματος λ = h/mv.
Ο Heisenberg διατύπωσε την αρχή της αβεβαιότητας: δεν μπορούμε να γνωρίζουμε ταυτόχρονα με ακρίβεια τη θέση και την ταχύτητα ενός ηλεκτρονίου. Αυτό δεν είναι τεχνικό πρόβλημα - είναι θεμελιώδης νόμος της φύσης!
Όλες αυτές οι ιδέες οδήγησαν στην εξίσωση του Schrödinger και στην έννοια των ατομικών τροχιακών - χώρων όπου έχουμε πιθανότητα να βρούμε ένα ηλεκτρόνιο.
💡 Βασική διαφορά: Δεν μιλάμε πλέον για συγκεκριμένες τροχιές, αλλά για περιοχές πιθανότητας!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Τα ατομικά τροχιακά είναι οι τρισδιάστατοι χώροι όπου έχουμε 99% πιθανότητα να βρούμε ένα ηλεκτρόνιο. Κάθε τροχιακό έχει τρία χαρακτηριστικά: μέγεθος, σχήμα και προσανατολισμό στο χώρο.
Μπορούμε να παραστήσουμε τα τροχιακά με τρεις τρόπους: με στίγματα (όσο πιο πυκνά, τόσο μεγαλύτερη η πιθανότητα), με καμπύλες που περικλείουν το 99% της πιθανότητας, ή με γραφικές παραστάσεις που δείχνουν πώς αλλάζει η πιθανότητα με την απόσταση από τον πυρήνα.
Η κυματοσυνάρτηση ψ από μόνη της δεν έχει φυσικό νόημα, αλλά το ψ² μας δίνει την πιθανότητα εύρεσης του ηλεκτρονίου σε κάθε σημείο. Αυτή είναι η βάση για να κατανοήσουμε τη δομή των ατόμων!
💡 Σημαντικό: Το τροχιακό δεν είναι η διαδρομή του ηλεκτρονίου, αλλά ο χώρος όπου πιθανότατα θα το βρούμε!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Κάθε ηλεκτρόνιο στο άτομο έχει μια μοναδική "διεύθυνση" που καθορίζεται από τέσσερις κβαντικούς αριθμούς. Είναι σαν το ταχυδρομικό κώδικα που καθορίζει ακριβώς πού βρίσκεται!
Ο κύριος κβαντικός αριθμός n (1,2,3...) δείχνει την απόσταση από τον πυρήνα και καθορίζει τη στιβάδα (K, L, M, N...). Όσο μεγαλύτερο το n, τόσο μεγαλύτερη η ενέργεια.
Ο αζιμουθιακός αριθμός l καθορίζει το σχήμα του τροχιακού: l=0→s (σφαιρικό), l=1→p (αλτήρας), l=2→d (πολύπλοκα σχήματα), l=3→f (ακόμα πιο πολύπλοκα). Το ζεύγος (n,l) καθορίζει την υποστιβάδα.
Ο μαγνητικός αριθμός ml δείχνει τον προσανατολισμό του τροχιακού. Ο spin ms (±½) δείχνει την "αυτοπεριστροφή" του ηλεκτρονίου.
💡 Θυμήσου: Η τετράδα (n,l,ml,ms) είναι μοναδική για κάθε ηλεκτρόνιο - δεν μπορούν δύο ηλεκτρόνια να έχουν την ίδια!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Τα s τροχιακά έχουν σφαιρική συμμετρία και η μέγιστη πιθανότητα εύρεσης ηλεκτρονίου είναι πάνω στον πυρήνα. Σε κάθε στιβάδα υπάρχει μόνο ένα s τροχιακό που χωράει 2 ηλεκτρόνια.
Τα p τροχιακά έχουν σχήμα αλτήρα και τρεις προσανατολισμούς (px, py, pz). Έχουν κομβική επιφάνεια - μια περιοχή όπου η πιθανότητα εύρεσης ηλεκτρονίου είναι μηδέν. Συνολικά χωράνε 6 ηλεκτρόνια (3 τροχιακά × 2 ηλεκτρόνια).
Τα d τροχιακά είναι 5 και χωράνε 10 ηλεκτρόνια, ενώ τα f τροχιακά είναι 7 και χωράνε 14 ηλεκτρόνια. Όσο αυξάνεται το l, τόσο πιο περίπλοκα γίνονται τα σχήματα.
Βασική διαφορά: στα s τροχιακά το ηλεκτρόνιο μπορεί να βρεθεί πάνω στον πυρήνα, ενώ στα p η πιθανότητα εκεί είναι μηδέν!
💡 Μνημονικό: s=1 τροχιακό, p=3 τροχιακά, d=5 τροχιακά, f=7 τροχιακά. Πολλαπλάσιασε επί 2 για τα ηλεκτρόνια!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Για να φτιάξεις τη σωστή ηλεκτρονιακή δομή ενός ατόμου, πρέπει να ακολουθήσεις τρεις βασικούς κανόνες που είναι σαν τους κανόνες ενός παιχνιδιού.
Η απαγορευτική αρχή του Pauli λέει ότι σε κάθε τροχιακό χωράνε μέχρι 2 ηλεκτρόνια με αντίθετο spin. Δεν μπορούν δύο ηλεκτρόνια να έχουν την ίδια τετράδα κβαντικών αριθμών.
Η αρχή ελάχιστης ενέργειας λέει ότι τα ηλεκτρόνια μπαίνουν πρώτα στα τροχιακά με τη μικρότερη ενέργεια. Η σειρά είναι: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d... Χρησιμοποίησε το άθροισμα για να θυμάσαι τη σειρά!
Προσοχή: όταν γράφεις κατιόντα, τα ηλεκτρόνια φεύγουν από την υποστιβάδα που γράφεται τελευταία (οριζόντια σειρά), όχι από αυτή που έχει τη μεγαλύτερη ενέργεια!
💡 Μνημονικός κανόνας: Χρησιμοποίησε το διάγραμμα με τις λοξές γραμμές για να θυμάσαι τη σειρά πλήρωσης!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Ο κανόνας του Hund είναι σαν να μοιράζεις καρέκλες σε μια αίθουσα: πρώτα κάθεται από ένας σε κάθε καρέκλα, μετά μπαίνει ο δεύτερος! Τα ηλεκτρόνια τοποθετούνται με παράλληλα spin σε τροχιακά ίδιας ενέργειας.
Στην πράξη: βάζεις πρώτα από ένα ηλεκτρόνιο (με θετικό spin) σε κάθε p, d ή f τροχιακό, και μετά συμπληρώνεις με το δεύτερο (αρνητικό spin).
Για παράδειγμα: C : 1s², 2s², 2p² → p: ↑ ↑ _ N : 1s², 2s², 2p³ → p: ↑ ↑ ↑ O : 1s², 2s², 2p⁴ → p: ↑↓ ↑ ↑
Για να γράψεις την πλήρη τετράδα κβαντικών αριθμών, ξεκινάς από το τελευταίο ηλεκτρόνιο. Η εξώτερη στιβάδα είναι αυτή με το μεγαλύτερο n και καθορίζει τις χημικές ιδιότητες!
💡 Tip: Ο κανόνας Hund εξηγεί γιατί ο άνθρακας έχει 2 μη ζευγαρωμένα ηλεκτρόνια και μπορεί να σχηματίσει 4 δεσμούς!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Ο περιοδικός πίνακας είναι η πιο έξυπνη εφεύρεση της χημείας! Τα 118 γνωστά στοιχεία είναι τοποθετημένα κατά αύξοντα ατομικό αριθμό, έτσι ώστε στοιχεία με παρόμοιες ιδιότητες να βρίσκονται στην ίδια στήλη.
Ο νόμος της περιοδικότητας λέει ότι οι ιδιότητες των στοιχείων επαναλαμβάνονται περιοδικά. Έχει 18 στήλες (ομάδες) και 7 σειρές (περιόδους). Οι σημαντικότερες ομάδες έχουν ονόματα: αλκάλια (IA), αλκαλικές γαίες (IIA), αλογόνα (VIIA), ευγενή αέρια (VIIIA).
Όλα τα ευγενή αέρια (εκτός το He) έχουν δομή ns²np⁶ - αυτό εξηγεί την σταθερότητά τους. Ο πίνακας χωρίζεται σε τομείς s, p, d, f ανάλογα με το πού μπαίνει το τελευταίο ηλεκτρόνιο.
Τομέας s: ομάδες IA-IIA (δομή ns¹ και ns²), Τομέας p: ομάδες IIIA-VIIIA (δομή ns²np¹⁻⁶), Τομέας d: μεταβατικά στοιχεία .
💡 Σημαντικό: Το He ανήκει στον τομέα s, παρότι βρίσκεται στην VIIIA ομάδα!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Για να βρεις τη θέση οποιουδήποτε στοιχείου, χρειάζεσαι μόνο την ηλεκτρονιακή του δομή! Είναι πιο εύκολο απ' ό,τι φαίνεται.
Το μέγιστο n δείχνει τον αριθμό της περιόδου. Για τους τομείς s και p, ο αριθμός ηλεκτρονίων της εξώτερης στιβάδας δίνει τον αριθμό της ομάδας (λατινικό σύστημα).
Για τον τομέα d: το μέγιστο n δίνει την περίοδο, ενώ ο αριθμός της ομάδας = ηλεκτρόνια σε ns + ηλεκτρόνια σε d.
Παράδειγμα: Te → 1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁴
Ο τομέας f περιλαμβάνει τις λανθανίδες (6η περίοδος) και ακτινίδες (7η περίοδος) - τα στοιχεία του παραρτήματος.
💡 Πρακτικό tip: Μάθε πρώτα να γράφεις δομές με βάση το προηγούμενο ευγενές αέριο - είναι πιο σύντομο!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
19
Έξυπνα Εργαλεία ΝΕΟ
Μετέτρεψε αυτές τις σημειώσεις σε: ✓ 50+ Ερωτήσεις Εξάσκησης ✓ Διαδραστικές Κάρτες Μνήμης ✓ Πλήρες Προσομοιωτικό Διαγώνισμα ✓ Σχέδια Δοκιμίου
App Store
Google Play
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS