Οι διαμοριακές δυνάμεις είναι οι ασθενέστερες αλληλεπιδράσεις που κρατάνε τα... Δες περισσότερα
Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟΕίναι δωρεάν!
Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Knowunity AI
Περισσότερα
Μαθήματα
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Δείξε όλα τα θέματα
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Δείξε όλα τα θέματα
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Δείξε όλα τα θέματα
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Δείξε όλα τα θέματα
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Δείξε όλα τα θέματα
355
•
Ενημερώθηκε Apr 18, 2026
•
Νικολίαツ
@_luv4yh
Οι διαμοριακές δυνάμεις είναι οι ασθενέστερες αλληλεπιδράσεις που κρατάνε τα... Δες περισσότερα

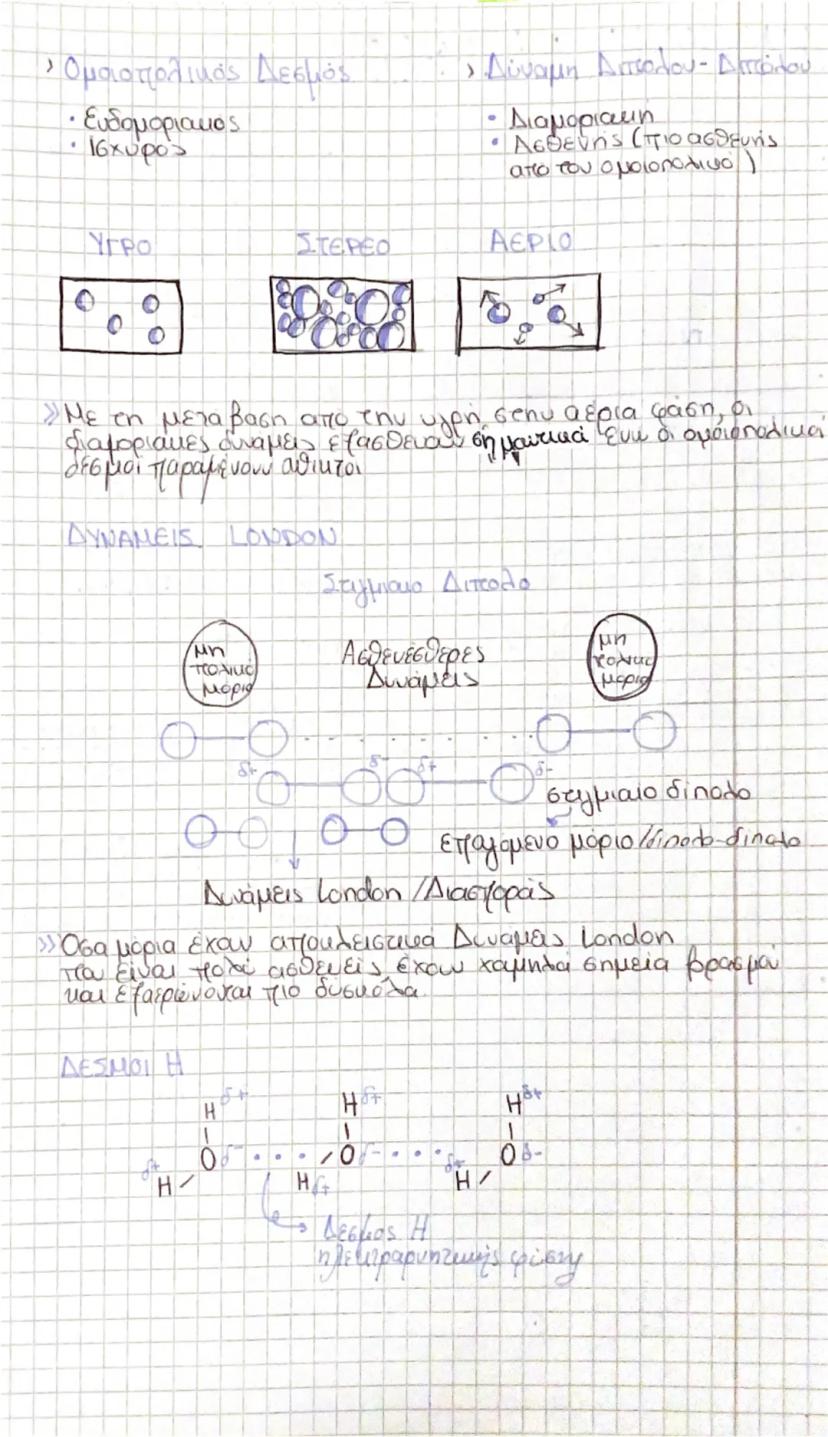






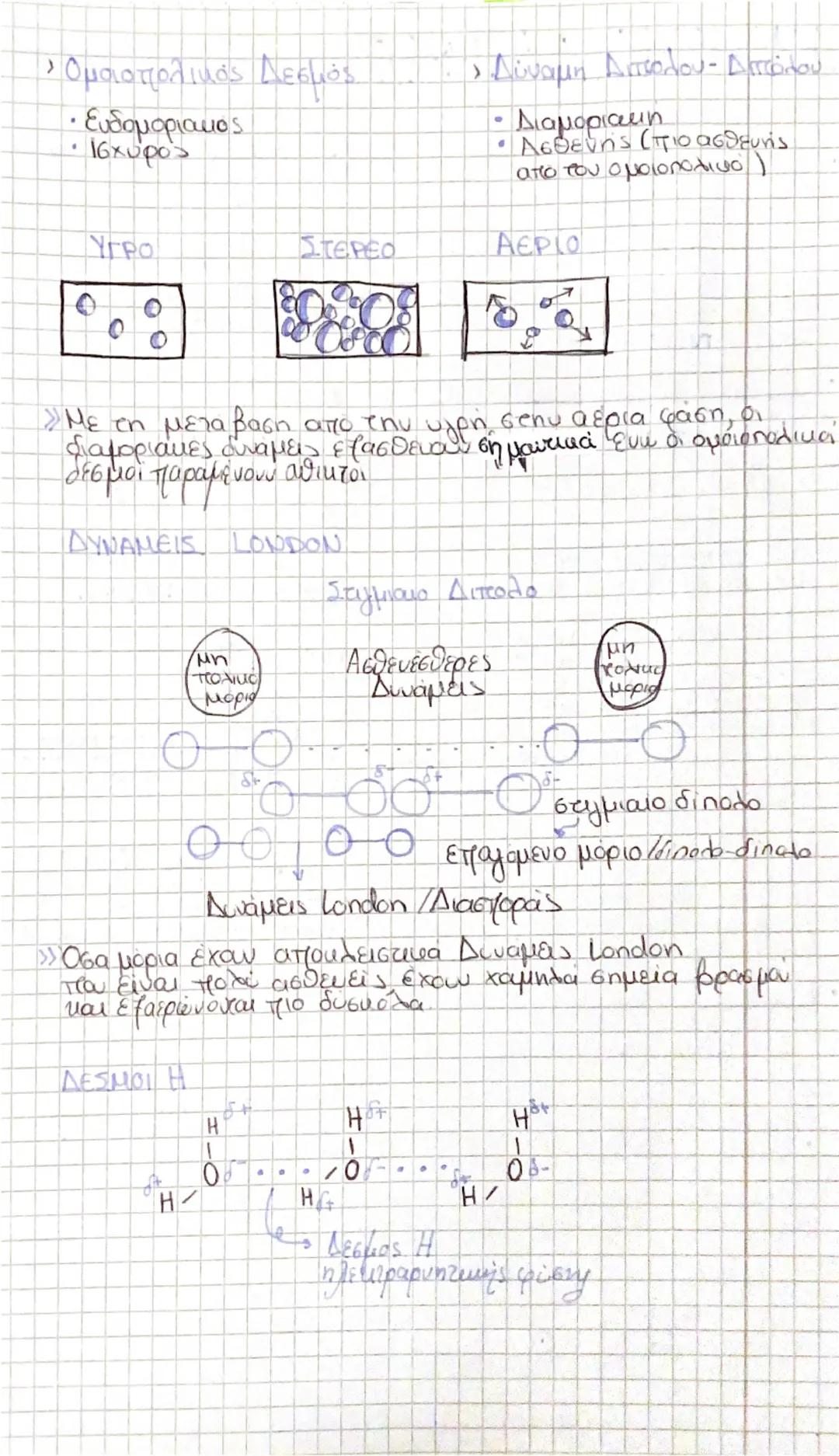
Όταν το νερό γίνεται ατμός, οι ομοιοπολικοί δεσμοί μέσα στα μόρια H₂O παραμένουν άθικτοι. Αυτό που αλλάζει είναι οι διαμοριακές δυνάμεις - οι πολύ ασθενέστερες δυνάμεις που κρατούν τα μόρια κοντά στην υγρή φάση.
Οι δυνάμεις London (ή διασποράς) είναι οι πιο αδύναμες από όλες και υπάρχουν σε όλα τα μόρια. Δημιουργούνται από στιγμιαία δίπολα που σχηματίζονται καθώς τα ηλεκτρόνια κινούνται γύρω από τον πυρήνα. Τα μόρια με απλούστερη δομή έχουν μόνο αυτές τις δυνάμεις, γι' αυτό έχουν χαμηλά σημεία βρασμού και εξατμίζονται εύκολα.
Οι δεσμοί υδρογόνου είναι πολύ πιο ισχυροί και σχηματίζονται όταν το υδρογόνο συνδέεται με F, O ή N. Στο νερό, η υψηλή ηλεκτραρνητικότητα του οξυγόνου δημιουργεί ισχυρούς δεσμούς H μεταξύ των μορίων.
Θυμήσου: Όσο ισχυρότερες οι διαμοριακές δυνάμεις, τόσο υψηλότερο το σημείο βρασμού της ουσίας.
Για να βρεις ποιες διαμοριακές δυνάμεις υπάρχουν μεταξύ των μορίων, ξεκινάς πάντα ελέγχοντας αν τα μόρια είναι πολικά ή μη πολικά.
Τα μη πολικά μόρια (όπως Ar, C₃H₈, CCl₄) έχουν μόνο δυνάμεις London. Το CCl₄ παρότι έχει πολωμένους δεσμούς, η συμμετρική τετραεδική δομή του κάνει τη συνολική διπολική ροπή μηδέν.
Τα πολικά μόρια (όπως HI, CHCl₃) έχουν δυνάμεις διπόλου-διπόλου συν δυνάμεις London. Το HI είναι πολικό λόγω της διαφοράς ηλεκτραρνητικότητας, ενώ το CHCl₃ δεν είναι συμμετρικό.
Όταν υπάρχει υδρογόνο συνδεμένο με F, O ή N (όπως στις αλκοόλες), σχηματίζονται δεσμοί υδρογόνου - οι ισχυρότεροι διαμοριακοί δεσμοί.
Tip: Πρώτα σχεδίαζε τη δομή Lewis, μετά ελέγχεις την πολικότητα και τέλος αποφασίζεις για τις διαμοριακές δυνάμεις.

Η σειρά ισχύος των διαμοριακών δυνάμεων είναι: Δυνάμεις London < Δίπολο-δίπολο < Δεσμοί υδρογόνου. Αυτή η σειρά καθορίζει άμεσα τα σημεία βρασμού των ουσιών.
Για παράδειγμα, στη σειρά N₂, O₂, NO, NH₃: Τα N₂ και O₂ είναι μη πολικά (μόνο London), το NO είναι πολικό , και το NH₃ έχει δεσμούς H. Άρα: Σ.Ζ.(NH₃) > Σ.Ζ.(NO) > Σ.Ζ.(O₂) > Σ.Ζ.(N₂).
Το μοριακό βάρος επηρεάζει επίσης την ισχύ των δυνάμεων London. Στα αλκάνια, όσο αυξάνει ο αριθμός των ατόμων άνθρακα, τόσο αυξάνει και το σημείο βρασμού.
Το σχήμα του μορίου έχει σημασία: τα ευθύγραμμα μόρια έχουν καλύτερη επαφή και ισχυρότερες δυνάμεις από τα διακλαδωμένα ισομερή τους.
Προσοχή: Οι δεσμοί υδρογόνου σχηματίζονται μόνο με F, O, N - όχι με άλλα στοιχεία!

Οι δυνάμεις London δημιουργούνται από τη γρήγορη κίνηση των ηλεκτρονίων που δημιουργεί στιγμιαία δίπολα. Αναπτύσσονται σε όλα τα μόρια και δεν έχουν συγκεκριμένη κατεύθυνση.
Η ισχύς των δυνάμεων London εξαρτάται από το μοριακό βάρος: όσο μεγαλύτερο το Mr, τόσο ισχυρότερες οι δυνάμεις. Στα ομόλογα αλκάνια βλέπουμε σταδιακή αύξηση του σημείου βρασμού με την προσθήκη ατόμων άνθρακα.
Το σχήμα του μορίου παίζει κρίσιμο ρόλο. Στα ισομερή του C₅H₁₂: το ευθύγραμμο έχει Σ.Ζ. 36°C, το διακλαδωμένο 28°C, και το πολύ διακλαδωμένο μόλις 9.5°C. Τα ευθύγραμμα μόρια "κολλάνε" καλύτερα μεταξύ τους.
Οι δεσμοί υδρογόνου απαιτούν συνδυασμό τριών χαρακτηριστικών: υψηλή ηλεκτραρνητικότητα (F>O>N), μικρό μέγεθος ατόμου, και ύπαρξη μη δεσμικών ζευγών ηλεκτρονίων.
Σημαντικό: Η ενέργεια των διαμοριακών δυνάμεων είναι πολύ μικρότερη από των ομοιοπολικών δεσμών .

Η ισχύς των διαμοριακών δυνάμεων καθορίζει άμεσα τα σημεία βρασμού. Όσο ισχυρότερες οι δυνάμεις, τόσο περισσότερη ενέργεια χρειάζεται για να τις σπάσουμε και να γίνει η ουσία αέριο.
Στις μη πολικές ουσίες με μόνο δυνάμεις London, η σειρά σημείων βρασμού ακολουθεί το μοριακό βάρος: F₂ < Cl₂ < Br₂ < I₂ και CH₄ < SiH₄ < GeH₄ < SnH₄.
Στις πολικές ουσίες, η σύγκριση γίνεται πιο περίπλοκη γιατί συνδυάζονται διαφορετικά είδη δυνάμεων. Για παράδειγμα: C₃H₈ < CH₃OCH₃ < CH₃Cl < CH₃CHO.
Όταν οι ουσίες έχουν παρόμοιο Mr, η σειρά ισχύος είναι: London < δίπολο-δίπολο < δεσμοί H. Αυτή η αρχή σε βοηθάει να προβλέπεις ποια ουσία θα έχει υψηλότερο σημείο βρασμού.
Πρακτικό tip: Σε άσκηση σύγκρισης, πρώτα ταξινόμησε τις ουσίες ανάλογα με τις διαμοριακές δυνάμεις τους, μετά κοίτα το Mr και το σχήμα.

Για να διατάξεις τις ενώσεις κατά αυξανόμενο σημείο βρασμού, ακολουθείς συστηματική μέθοδο σύγκρισης.
Πρώτα ομαδοποιείς ανάλογα με τις διαμοριακές δυνάμεις: Οι υδρογονάνθρακες Α και Γ έχουν μόνο London, ο αιθέρας Ε έχει δίπολο-δίπολο + London, οι αλκοόλες Β και Δ έχουν δεσμούς H.
Μεταξύ των υδρογοναθράκων με ίδιο Mr (Α και Γ): το ευθύγραμμο Α έχει καλύτερη επαφή μορίων από το διακλαδωμένο Γ, άρα Σ.Ζ.(Α) > Σ.Ζ.(Γ).
Στις αλκοόλες Β και Δ: το Β έχει μεγαλύτερο Mr από το Δ, άρα ισχυρότερους δεσμούς H και υψηλότερο σημείο βρασμού.
Η τελική σειρά είναι: Γ < Α < Ε < Δ < Β. Παρατήρησε ότι ακόμα και η μικρότερη αλκοόλη (Δ) έχει υψηλότερο σημείο βρασμού από τον αιθέρα (Ε) λόγω των δεσμών H.
Στρατηγική: Πάντα ξεκινάς από τον τύπο διαμοριακών δυνάμεων, μετά συγκρίνεις Mr και σχήμα μορίου.

Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
App Store
Google Play
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Νικολίαツ
@_luv4yh
Οι διαμοριακές δυνάμεις είναι οι ασθενέστερες αλληλεπιδράσεις που κρατάνε τα μόρια κοντά και επηρεάζουν τις ιδιότητες των ουσιών. Αντίθετα με τους ομοιοπολικούς δεσμούς που "σπάνε" μέσα στα μόρια, οι διαμοριακές δυνάμεις επηρεάζουν πώς τα μόρια συμπεριφέρονται μεταξύ τους στις διαφορετικές... Δες περισσότερα

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Όταν το νερό γίνεται ατμός, οι ομοιοπολικοί δεσμοί μέσα στα μόρια H₂O παραμένουν άθικτοι. Αυτό που αλλάζει είναι οι διαμοριακές δυνάμεις - οι πολύ ασθενέστερες δυνάμεις που κρατούν τα μόρια κοντά στην υγρή φάση.
Οι δυνάμεις London (ή διασποράς) είναι οι πιο αδύναμες από όλες και υπάρχουν σε όλα τα μόρια. Δημιουργούνται από στιγμιαία δίπολα που σχηματίζονται καθώς τα ηλεκτρόνια κινούνται γύρω από τον πυρήνα. Τα μόρια με απλούστερη δομή έχουν μόνο αυτές τις δυνάμεις, γι' αυτό έχουν χαμηλά σημεία βρασμού και εξατμίζονται εύκολα.
Οι δεσμοί υδρογόνου είναι πολύ πιο ισχυροί και σχηματίζονται όταν το υδρογόνο συνδέεται με F, O ή N. Στο νερό, η υψηλή ηλεκτραρνητικότητα του οξυγόνου δημιουργεί ισχυρούς δεσμούς H μεταξύ των μορίων.
Θυμήσου: Όσο ισχυρότερες οι διαμοριακές δυνάμεις, τόσο υψηλότερο το σημείο βρασμού της ουσίας.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Για να βρεις ποιες διαμοριακές δυνάμεις υπάρχουν μεταξύ των μορίων, ξεκινάς πάντα ελέγχοντας αν τα μόρια είναι πολικά ή μη πολικά.
Τα μη πολικά μόρια (όπως Ar, C₃H₈, CCl₄) έχουν μόνο δυνάμεις London. Το CCl₄ παρότι έχει πολωμένους δεσμούς, η συμμετρική τετραεδική δομή του κάνει τη συνολική διπολική ροπή μηδέν.
Τα πολικά μόρια (όπως HI, CHCl₃) έχουν δυνάμεις διπόλου-διπόλου συν δυνάμεις London. Το HI είναι πολικό λόγω της διαφοράς ηλεκτραρνητικότητας, ενώ το CHCl₃ δεν είναι συμμετρικό.
Όταν υπάρχει υδρογόνο συνδεμένο με F, O ή N (όπως στις αλκοόλες), σχηματίζονται δεσμοί υδρογόνου - οι ισχυρότεροι διαμοριακοί δεσμοί.
Tip: Πρώτα σχεδίαζε τη δομή Lewis, μετά ελέγχεις την πολικότητα και τέλος αποφασίζεις για τις διαμοριακές δυνάμεις.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Η σειρά ισχύος των διαμοριακών δυνάμεων είναι: Δυνάμεις London < Δίπολο-δίπολο < Δεσμοί υδρογόνου. Αυτή η σειρά καθορίζει άμεσα τα σημεία βρασμού των ουσιών.
Για παράδειγμα, στη σειρά N₂, O₂, NO, NH₃: Τα N₂ και O₂ είναι μη πολικά (μόνο London), το NO είναι πολικό , και το NH₃ έχει δεσμούς H. Άρα: Σ.Ζ.(NH₃) > Σ.Ζ.(NO) > Σ.Ζ.(O₂) > Σ.Ζ.(N₂).
Το μοριακό βάρος επηρεάζει επίσης την ισχύ των δυνάμεων London. Στα αλκάνια, όσο αυξάνει ο αριθμός των ατόμων άνθρακα, τόσο αυξάνει και το σημείο βρασμού.
Το σχήμα του μορίου έχει σημασία: τα ευθύγραμμα μόρια έχουν καλύτερη επαφή και ισχυρότερες δυνάμεις από τα διακλαδωμένα ισομερή τους.
Προσοχή: Οι δεσμοί υδρογόνου σχηματίζονται μόνο με F, O, N - όχι με άλλα στοιχεία!

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Οι δυνάμεις London δημιουργούνται από τη γρήγορη κίνηση των ηλεκτρονίων που δημιουργεί στιγμιαία δίπολα. Αναπτύσσονται σε όλα τα μόρια και δεν έχουν συγκεκριμένη κατεύθυνση.
Η ισχύς των δυνάμεων London εξαρτάται από το μοριακό βάρος: όσο μεγαλύτερο το Mr, τόσο ισχυρότερες οι δυνάμεις. Στα ομόλογα αλκάνια βλέπουμε σταδιακή αύξηση του σημείου βρασμού με την προσθήκη ατόμων άνθρακα.
Το σχήμα του μορίου παίζει κρίσιμο ρόλο. Στα ισομερή του C₅H₁₂: το ευθύγραμμο έχει Σ.Ζ. 36°C, το διακλαδωμένο 28°C, και το πολύ διακλαδωμένο μόλις 9.5°C. Τα ευθύγραμμα μόρια "κολλάνε" καλύτερα μεταξύ τους.
Οι δεσμοί υδρογόνου απαιτούν συνδυασμό τριών χαρακτηριστικών: υψηλή ηλεκτραρνητικότητα (F>O>N), μικρό μέγεθος ατόμου, και ύπαρξη μη δεσμικών ζευγών ηλεκτρονίων.
Σημαντικό: Η ενέργεια των διαμοριακών δυνάμεων είναι πολύ μικρότερη από των ομοιοπολικών δεσμών .

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Η ισχύς των διαμοριακών δυνάμεων καθορίζει άμεσα τα σημεία βρασμού. Όσο ισχυρότερες οι δυνάμεις, τόσο περισσότερη ενέργεια χρειάζεται για να τις σπάσουμε και να γίνει η ουσία αέριο.
Στις μη πολικές ουσίες με μόνο δυνάμεις London, η σειρά σημείων βρασμού ακολουθεί το μοριακό βάρος: F₂ < Cl₂ < Br₂ < I₂ και CH₄ < SiH₄ < GeH₄ < SnH₄.
Στις πολικές ουσίες, η σύγκριση γίνεται πιο περίπλοκη γιατί συνδυάζονται διαφορετικά είδη δυνάμεων. Για παράδειγμα: C₃H₈ < CH₃OCH₃ < CH₃Cl < CH₃CHO.
Όταν οι ουσίες έχουν παρόμοιο Mr, η σειρά ισχύος είναι: London < δίπολο-δίπολο < δεσμοί H. Αυτή η αρχή σε βοηθάει να προβλέπεις ποια ουσία θα έχει υψηλότερο σημείο βρασμού.
Πρακτικό tip: Σε άσκηση σύγκρισης, πρώτα ταξινόμησε τις ουσίες ανάλογα με τις διαμοριακές δυνάμεις τους, μετά κοίτα το Mr και το σχήμα.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Για να διατάξεις τις ενώσεις κατά αυξανόμενο σημείο βρασμού, ακολουθείς συστηματική μέθοδο σύγκρισης.
Πρώτα ομαδοποιείς ανάλογα με τις διαμοριακές δυνάμεις: Οι υδρογονάνθρακες Α και Γ έχουν μόνο London, ο αιθέρας Ε έχει δίπολο-δίπολο + London, οι αλκοόλες Β και Δ έχουν δεσμούς H.
Μεταξύ των υδρογοναθράκων με ίδιο Mr (Α και Γ): το ευθύγραμμο Α έχει καλύτερη επαφή μορίων από το διακλαδωμένο Γ, άρα Σ.Ζ.(Α) > Σ.Ζ.(Γ).
Στις αλκοόλες Β και Δ: το Β έχει μεγαλύτερο Mr από το Δ, άρα ισχυρότερους δεσμούς H και υψηλότερο σημείο βρασμού.
Η τελική σειρά είναι: Γ < Α < Ε < Δ < Β. Παρατήρησε ότι ακόμα και η μικρότερη αλκοόλη (Δ) έχει υψηλότερο σημείο βρασμού από τον αιθέρα (Ε) λόγω των δεσμών H.
Στρατηγική: Πάντα ξεκινάς από τον τύπο διαμοριακών δυνάμεων, μετά συγκρίνεις Mr και σχήμα μορίου.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
5
Έξυπνα Εργαλεία ΝΕΟ
Μετέτρεψε αυτές τις σημειώσεις σε: ✓ 50+ Ερωτήσεις Εξάσκησης ✓ Διαδραστικές Κάρτες Μνήμης ✓ Πλήρες Προσομοιωτικό Διαγώνισμα ✓ Σχέδια Δοκιμίου
App Store
Google Play
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS