Η θεωρία δεσμού σθένους είναι μια από τις πιο σημαντικές... Δες περισσότερα
Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟΕίναι δωρεάν!
Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Knowunity AI
Περισσότερα
Μαθήματα
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Δείξε όλα τα θέματα
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Δείξε όλα τα θέματα
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Δείξε όλα τα θέματα
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Δείξε όλα τα θέματα
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Δείξε όλα τα θέματα
360
•
Ενημερώθηκε Apr 19, 2026
•
3Lithio
@3lithio
Η θεωρία δεσμού σθένους είναι μια από τις πιο σημαντικές... Δες περισσότερα


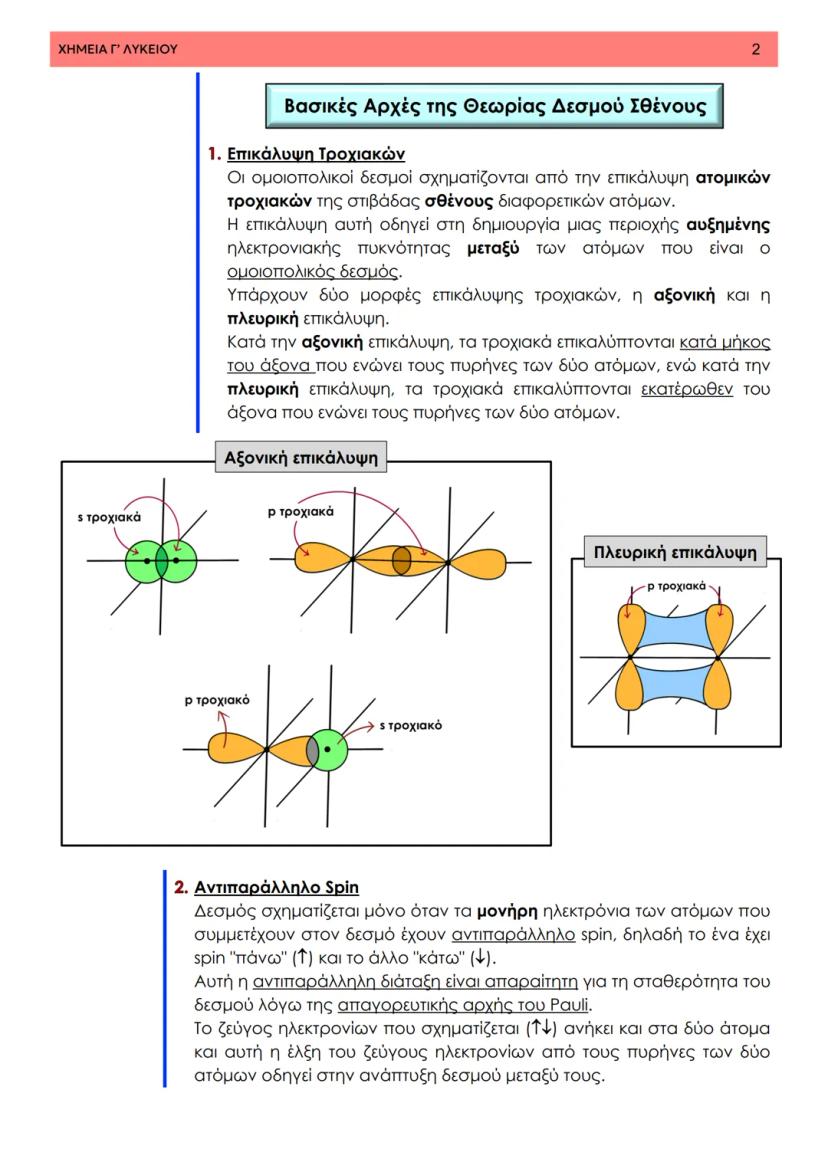





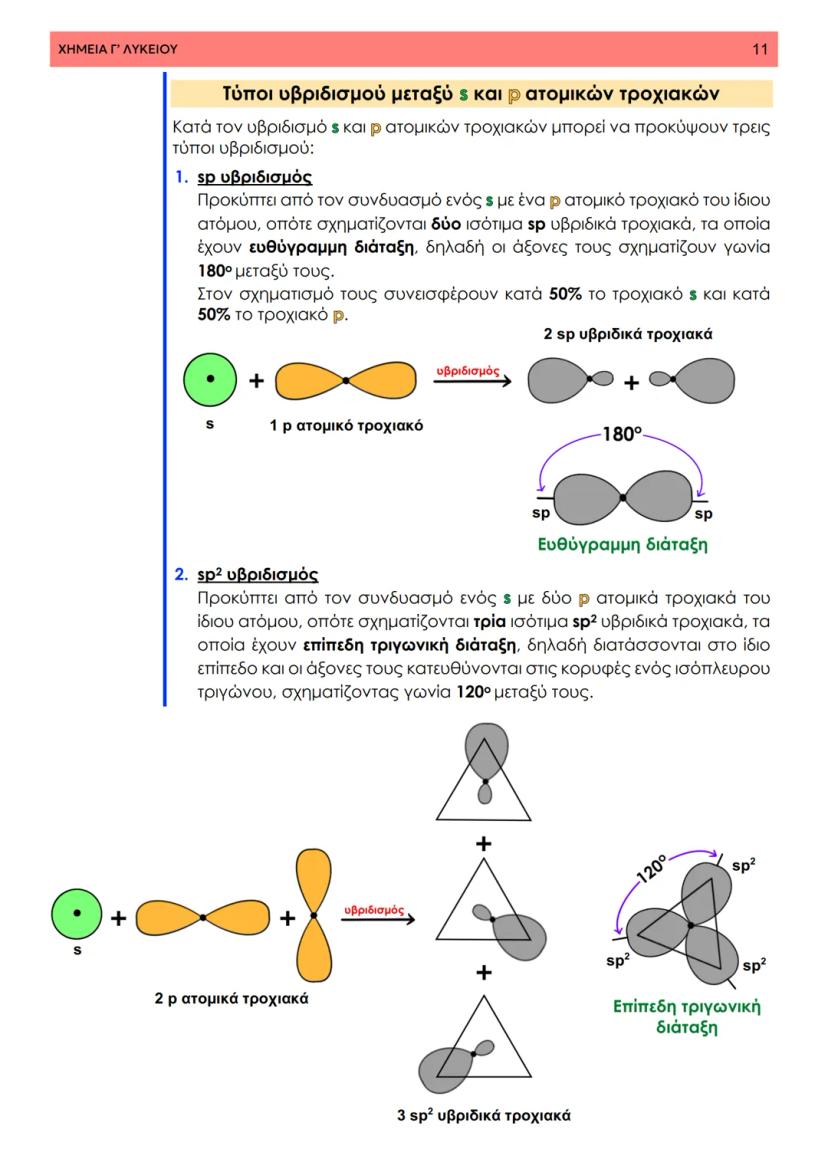
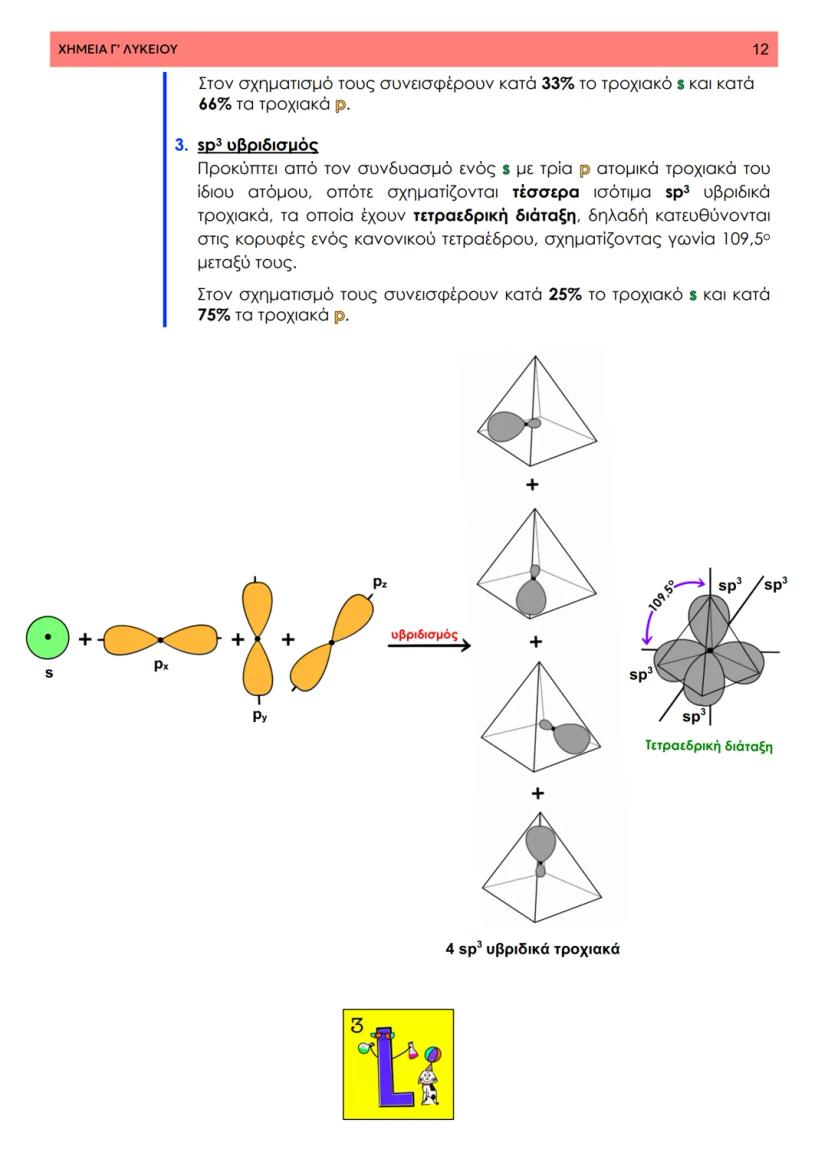
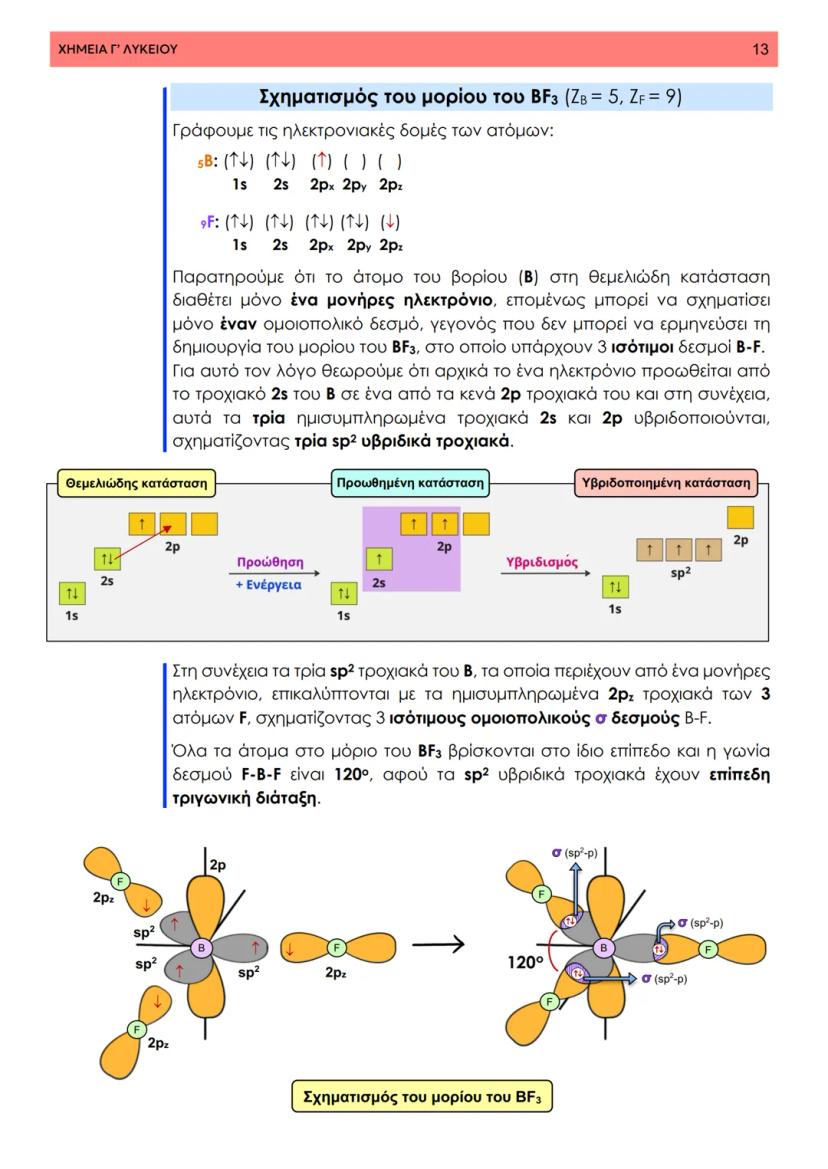

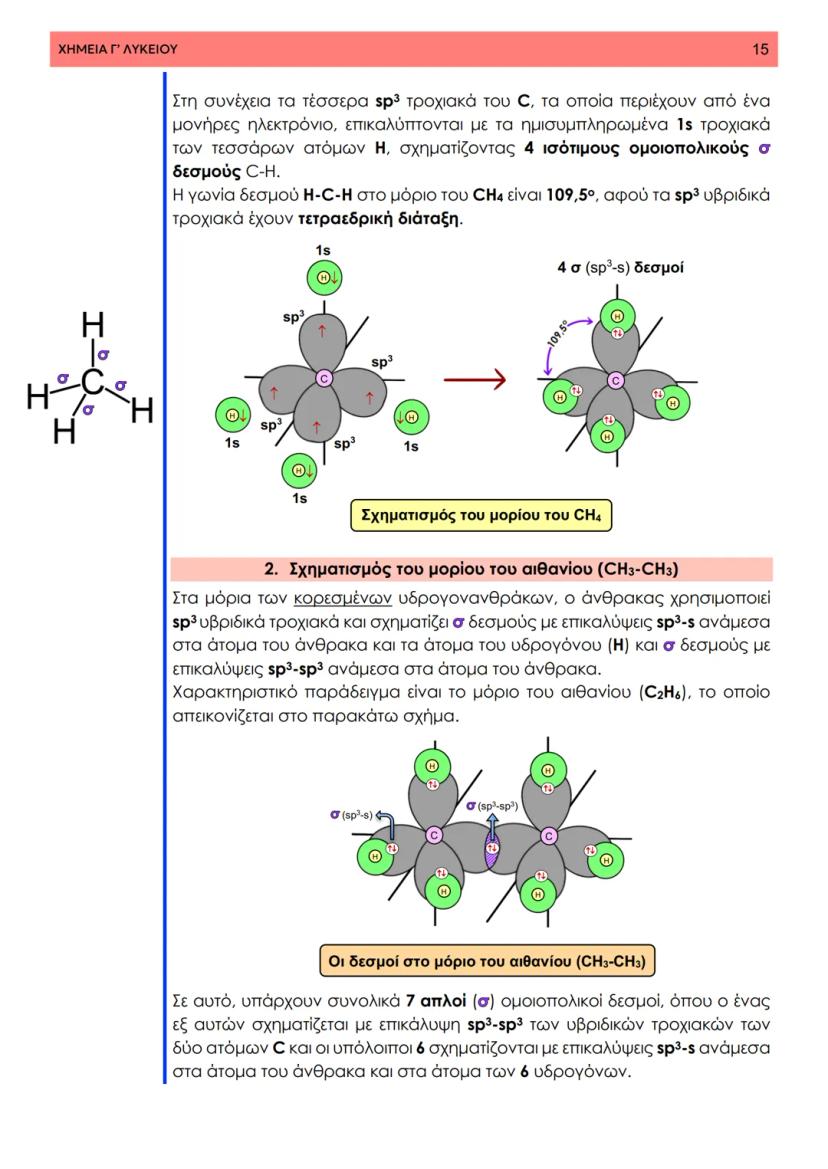
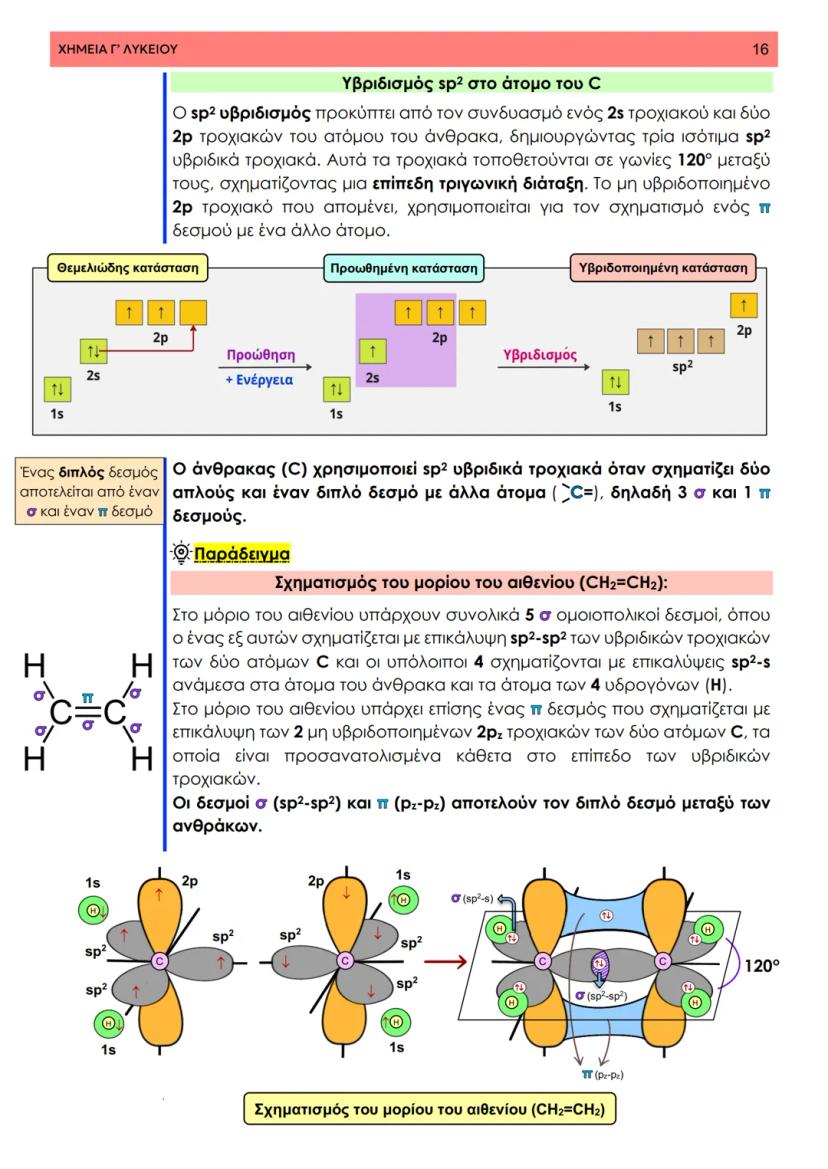
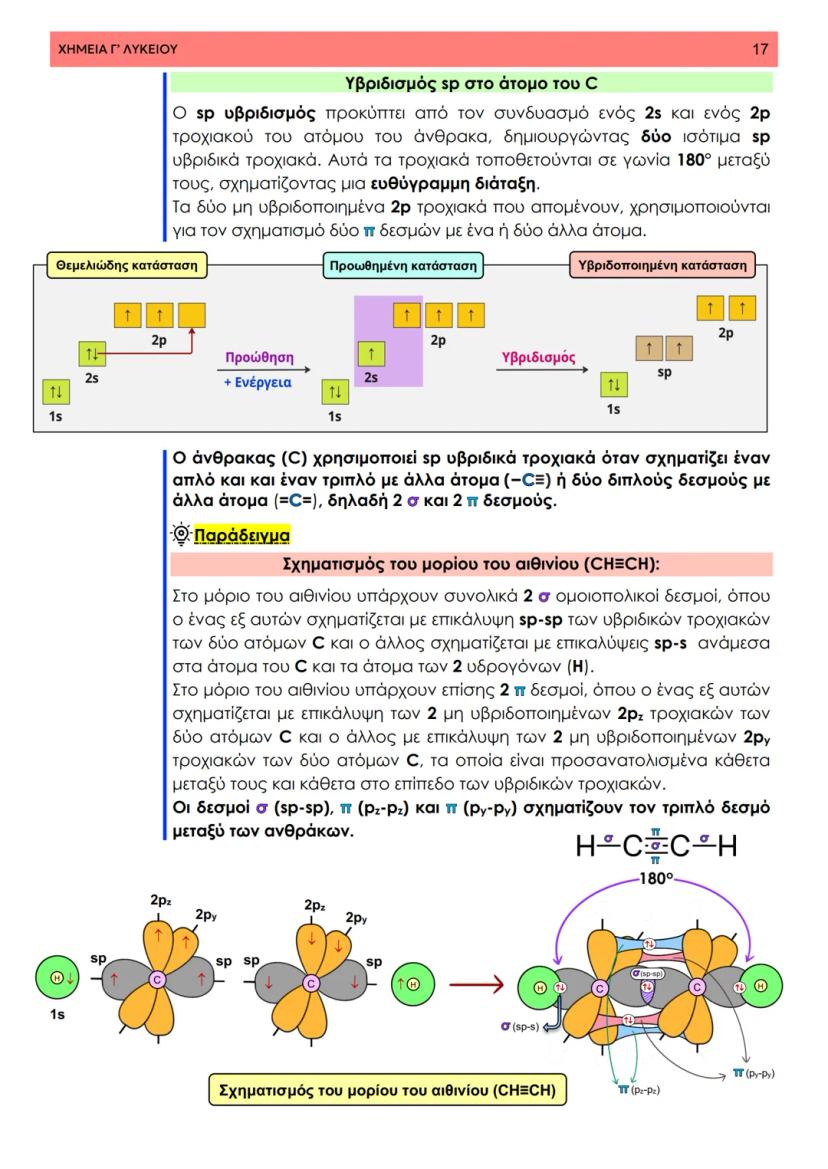
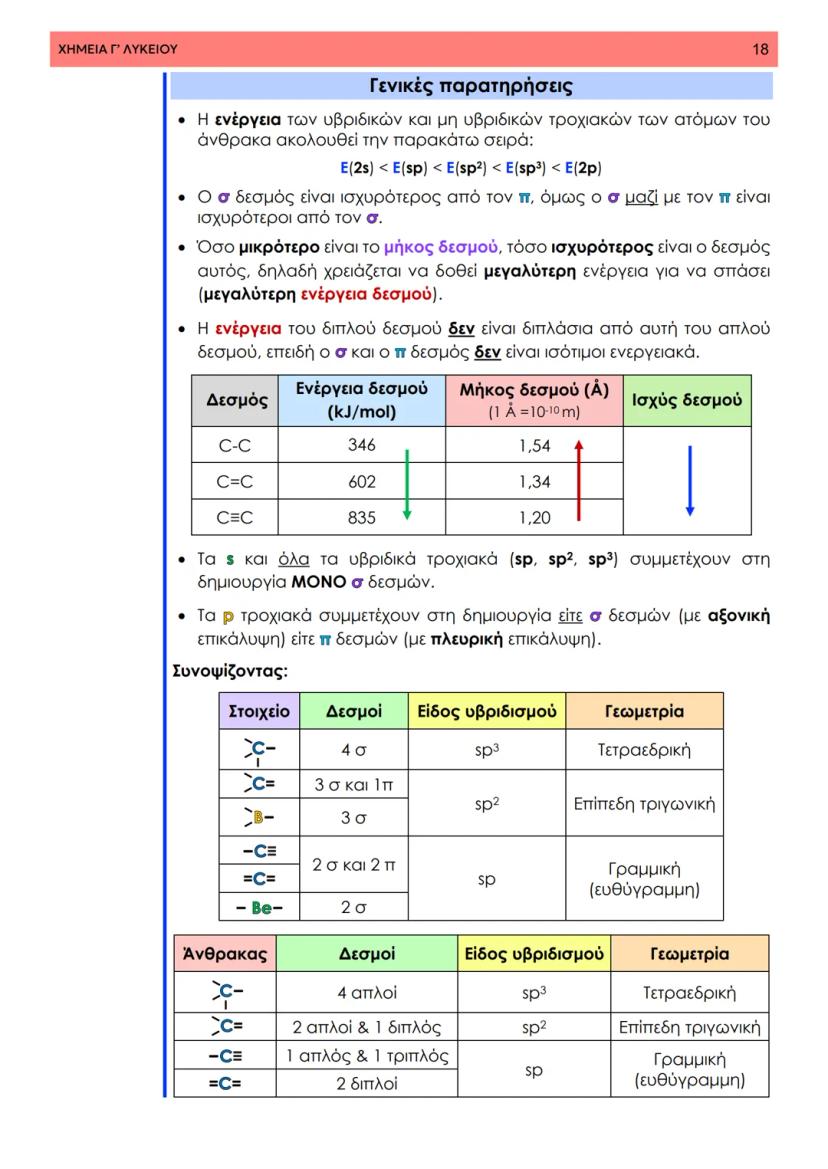
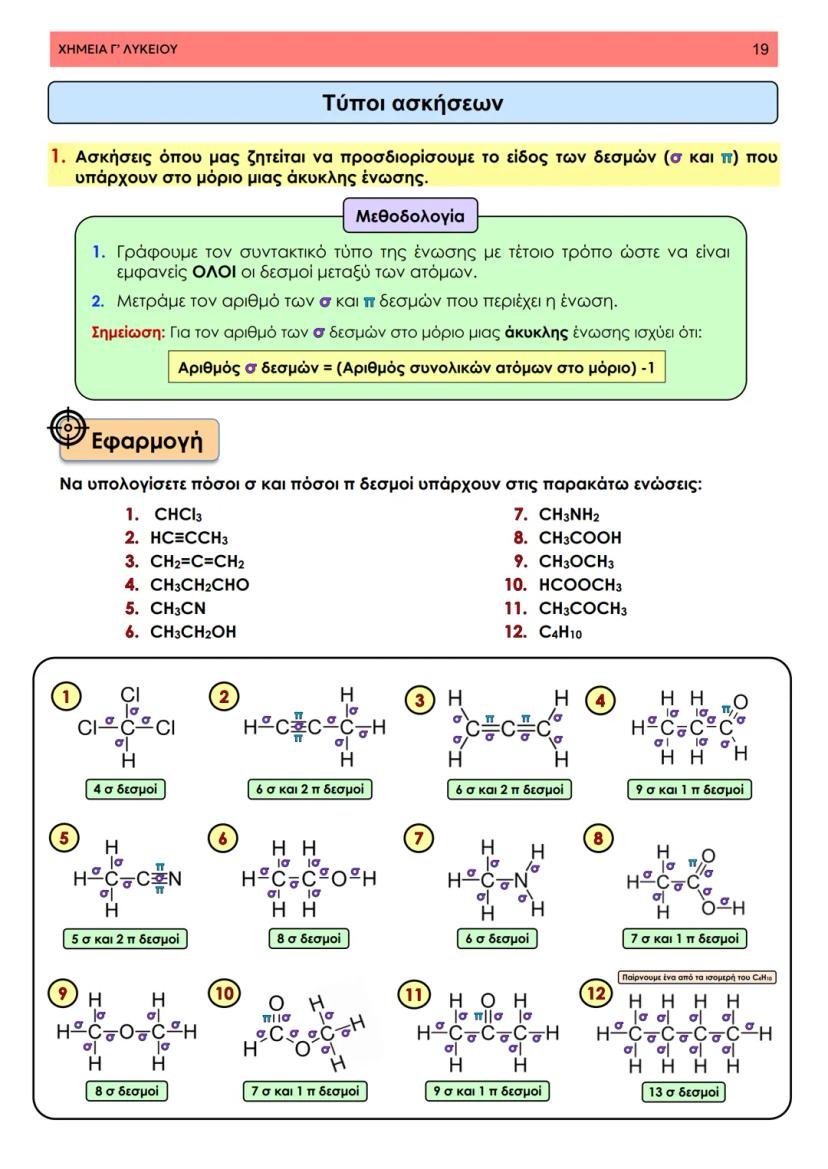
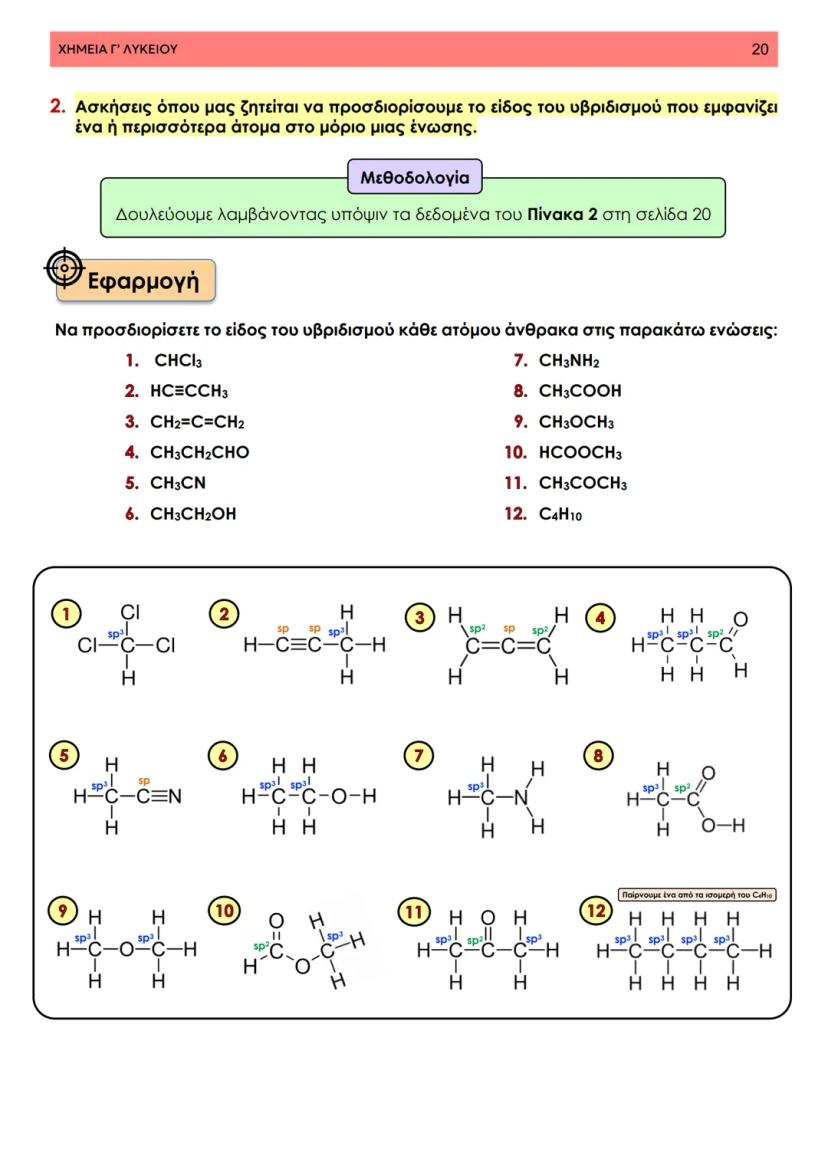
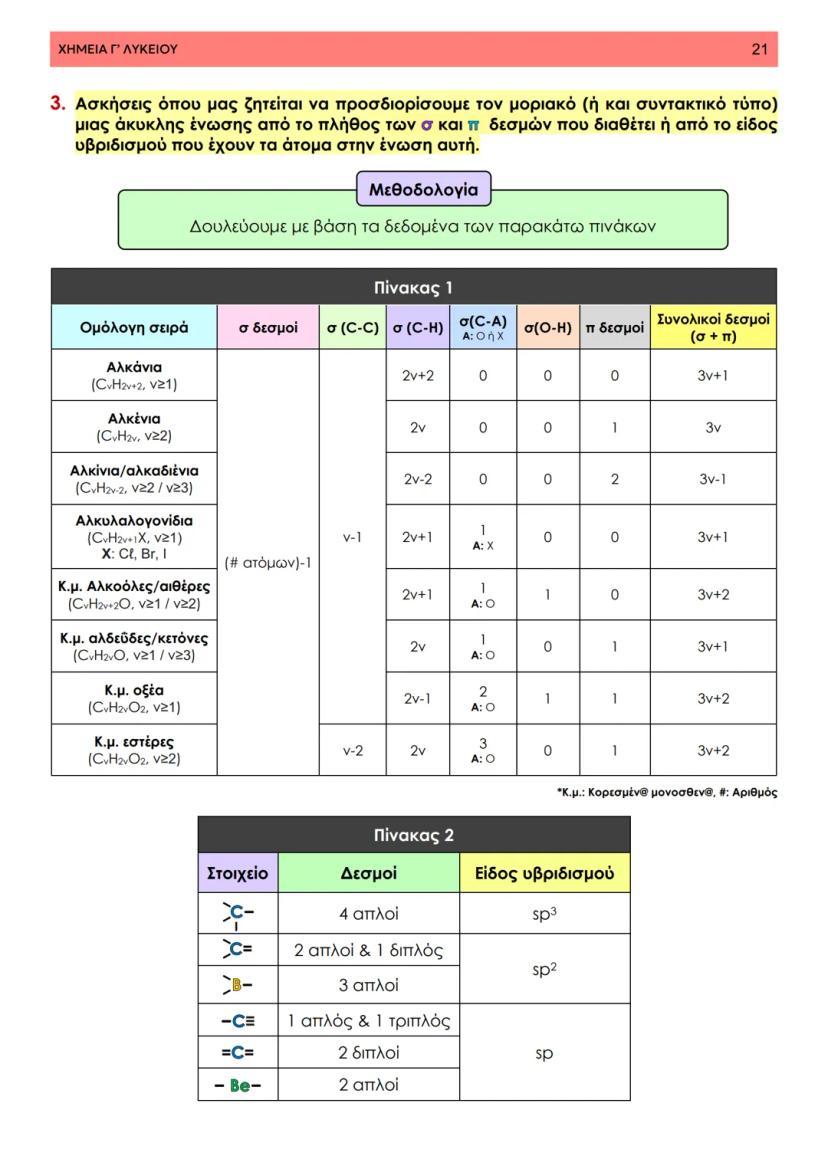

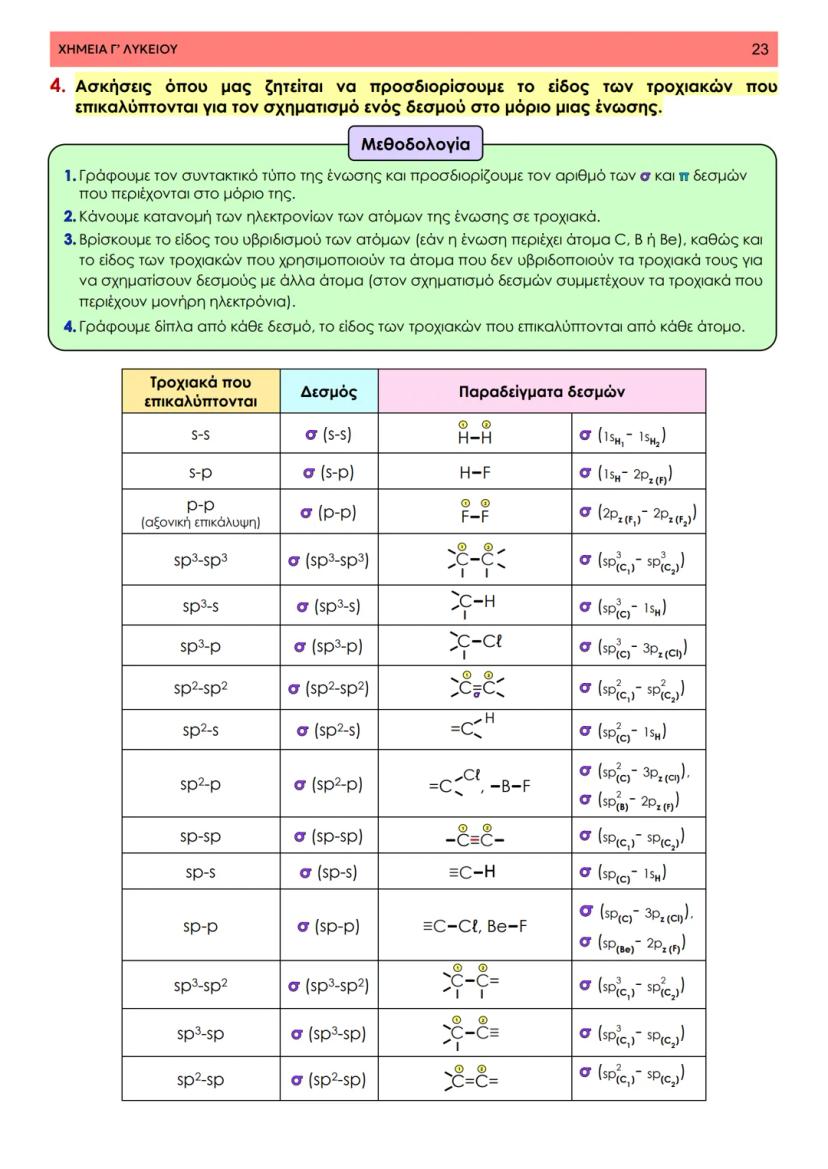
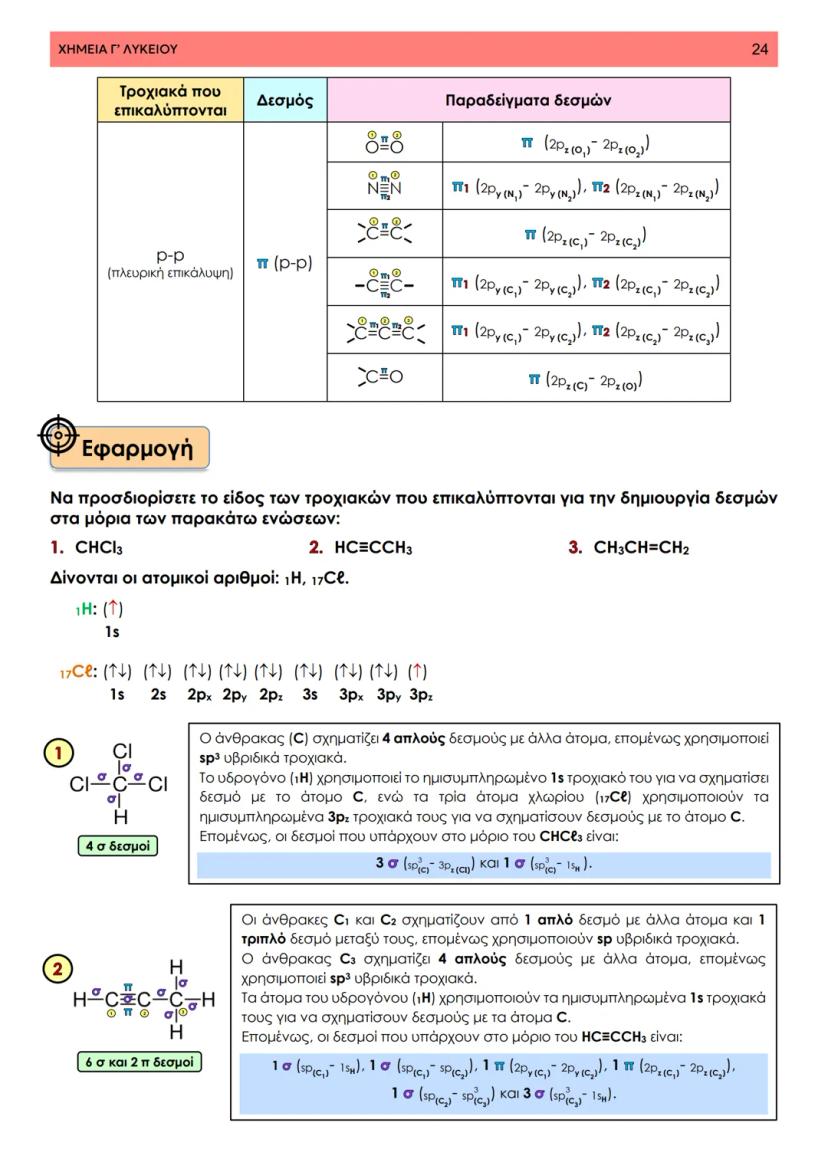
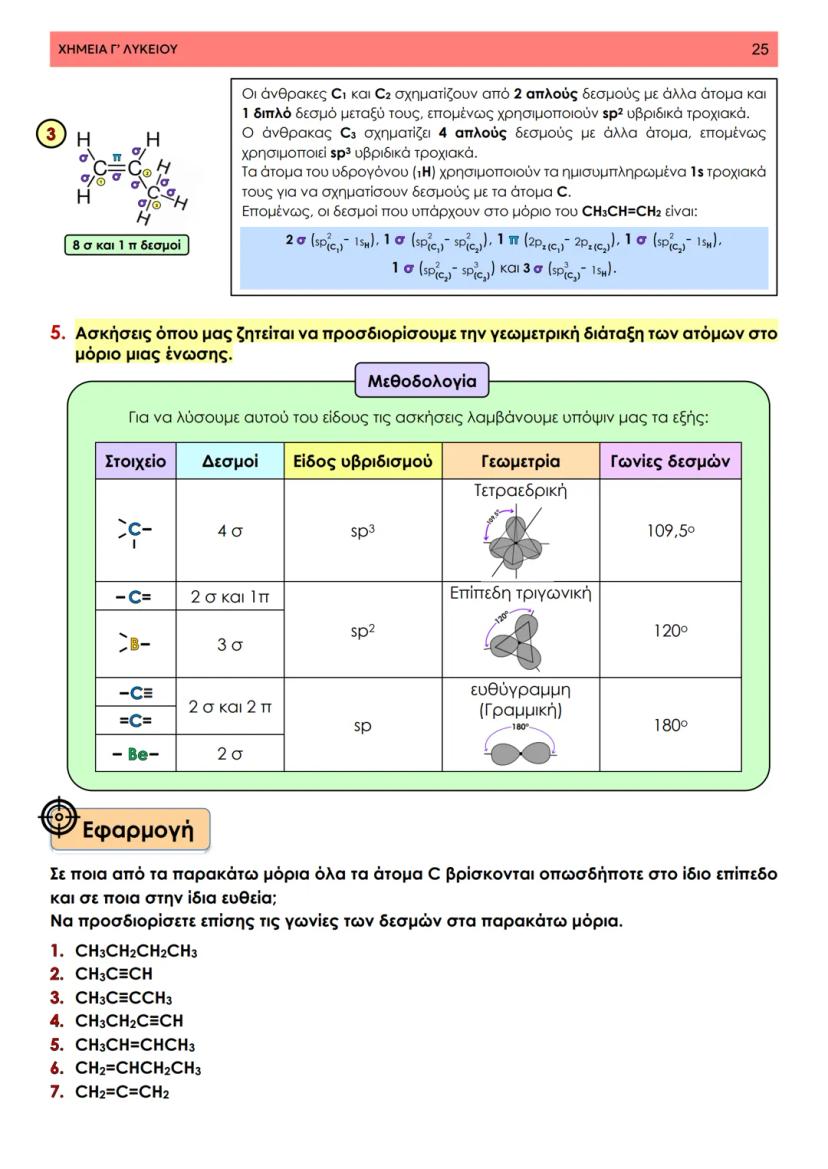



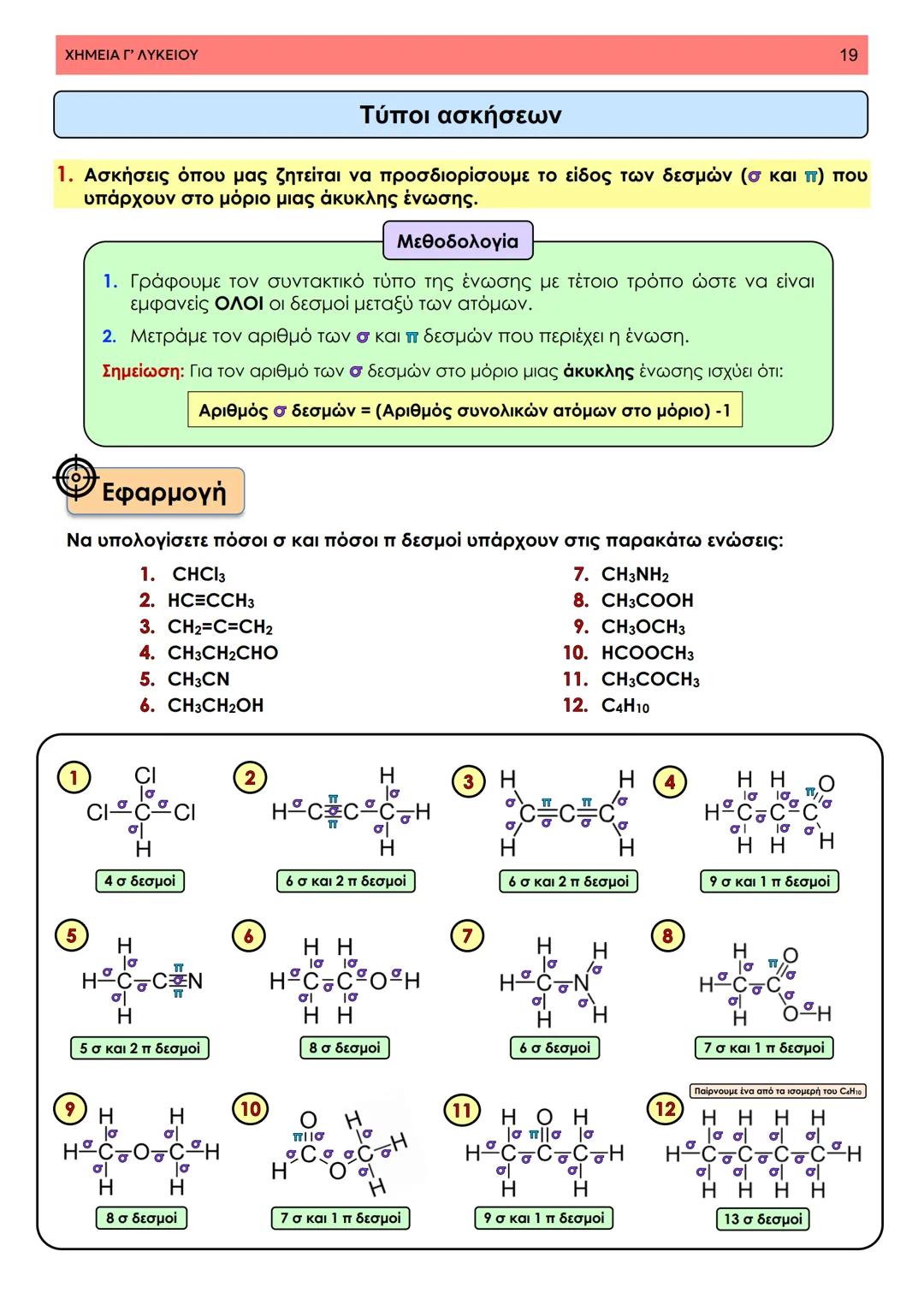
Στη θεωρία δεσμού σθένους, ο ομοιοπολικός δεσμός προκύπτει από την επικάλυψη ατομικών τροχιακών δύο ατόμων που περιέχουν μονήρη ηλεκτρόνια με αντιπαράλληλο spin. Φανταστείτε δύο άτομα που πλησιάζουν το ένα στο άλλο - τα τροχιακά τους επικαλύπτονται και δημιουργούν μια περιοχή αυξημένης ηλεκτρονιακής πυκνότητας.
Αυτή η επικάλυψη είναι που κρατάει τα άτομα μαζί, μειώνοντας την ενέργεια του συστήματος. Το αποτέλεσμα; Το μόριο γίνεται πιο σταθερό από τα μεμονωμένα άτομα.
Θυμηθείτε: Οι δεσμοί σχηματίζονται μόνο με ηλεκτρόνια που έχουν αντιπαράλληλο spin (↑↓), όπως ορίζει η απαγορευτική αρχή του Pauli.

Υπάρχουν δύο βασικοί τρόποι επικάλυψης τροχιακών. Η αξονική επικάλυψη γίνεται κατά μήκος του άξονα που ενώνει τους πυρήνες, ενώ η πλευρική επικάλυψη γίνεται εκατέρωθεν αυτού του άξονα.
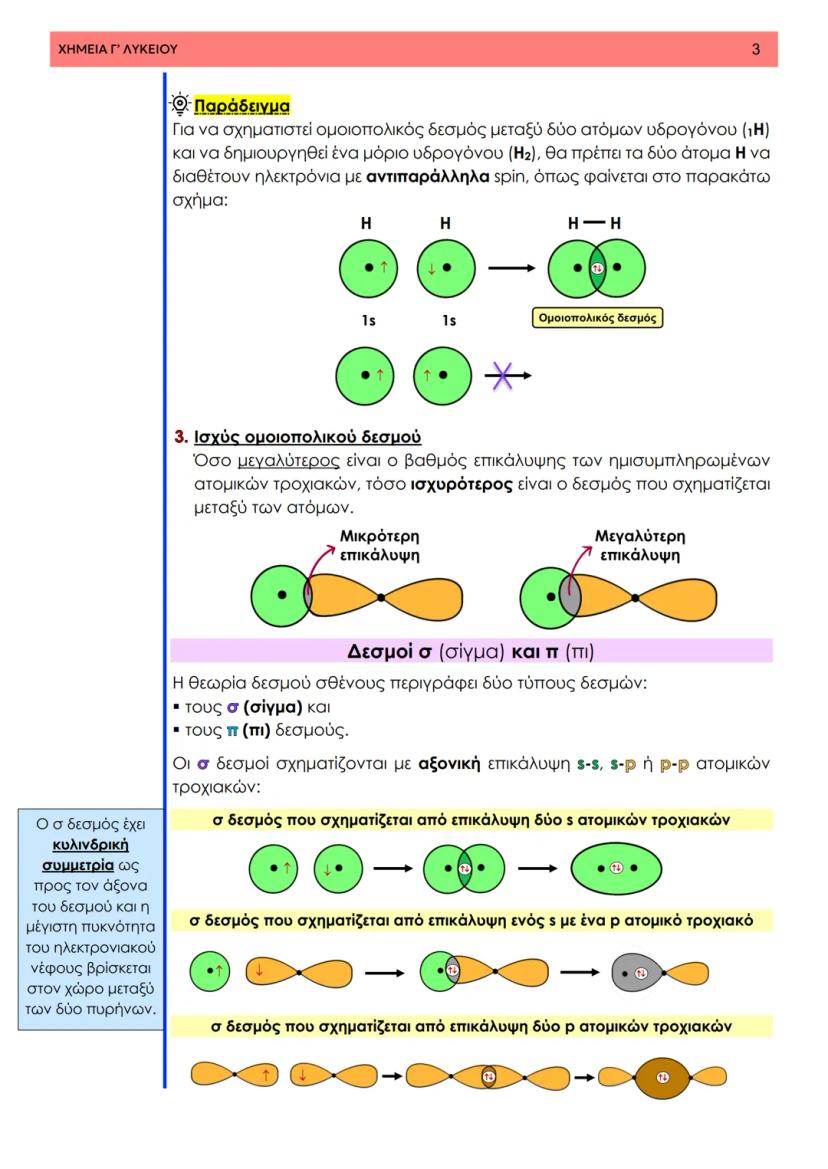
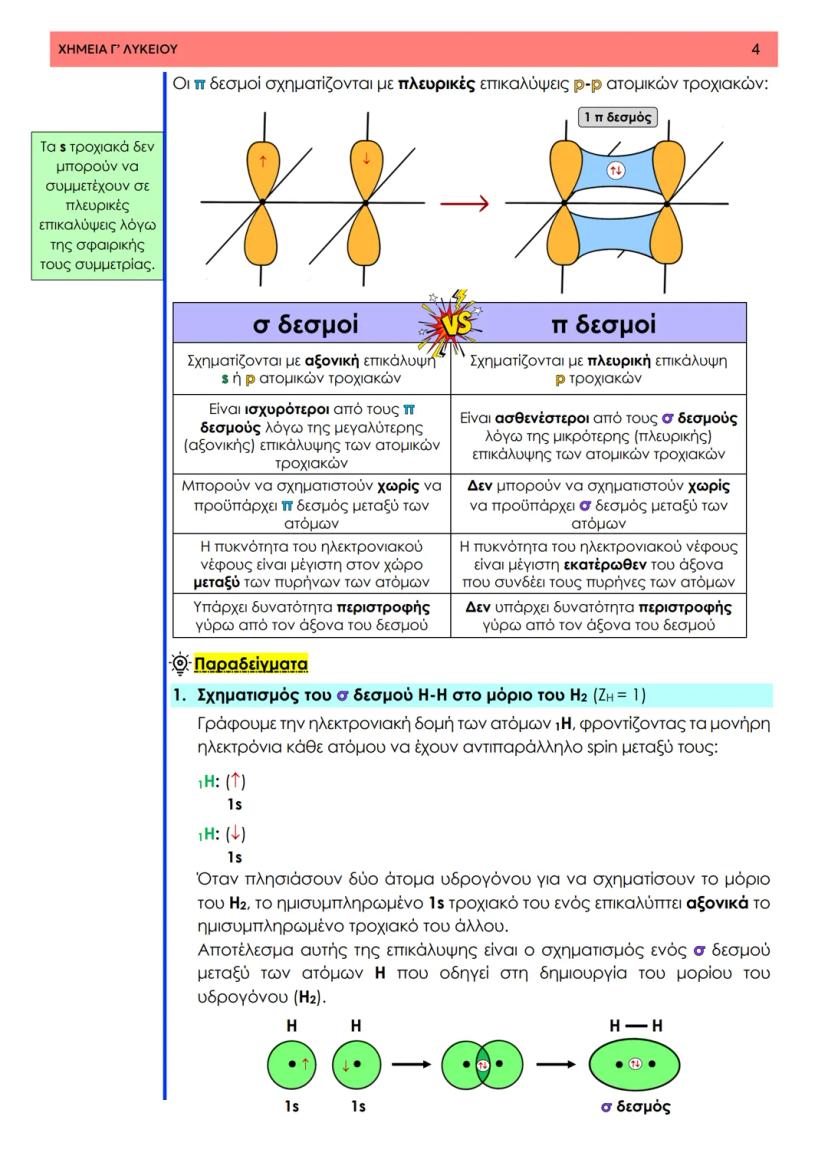
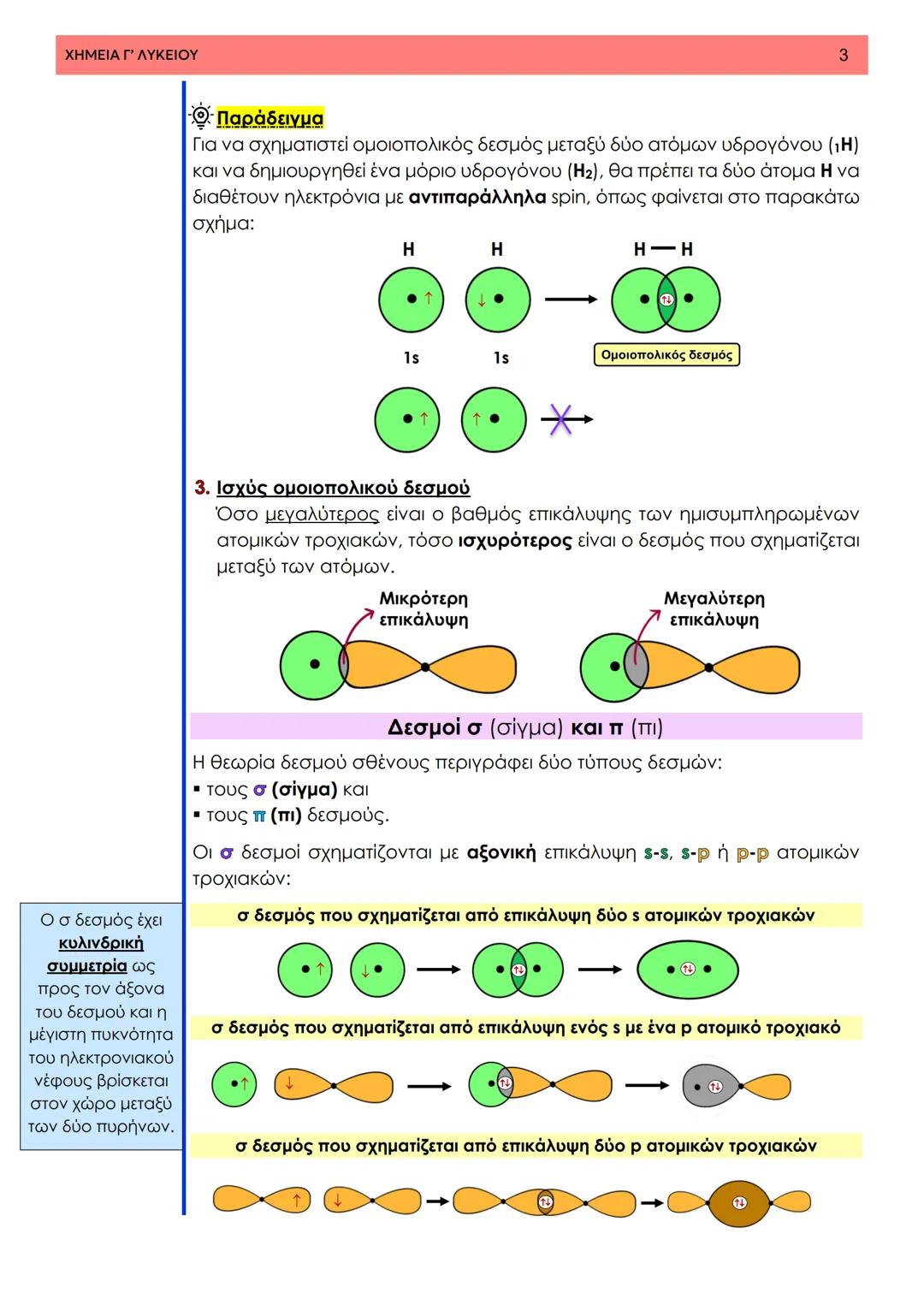
Αυτοί οι τρόποι επικάλυψης δημιουργούν δύο διαφορετικούς τύπους δεσμών. Οι σ (σίγμα) δεσμοί προκύπτουν από αξονική επικάλυψη s-s, s-p ή p-p τροχιακών και είναι ισχυρότεροι. Οι π (πι) δεσμοί σχηματίζονται από πλευρική επικάλυψη p τροχιακών και είναι ασθενέστεροι.
Σημαντικό: Όσο μεγαλύτερη είναι η επικάλυψη των τροχιακών, τόσο ισχυρότερος είναι ο δεσμός που προκύπτει.
Οι π δεσμοί δεν μπορούν να υπάρξουν χωρίς να προϋπάρχει σ δεσμός μεταξύ των ίδιων ατόμων.
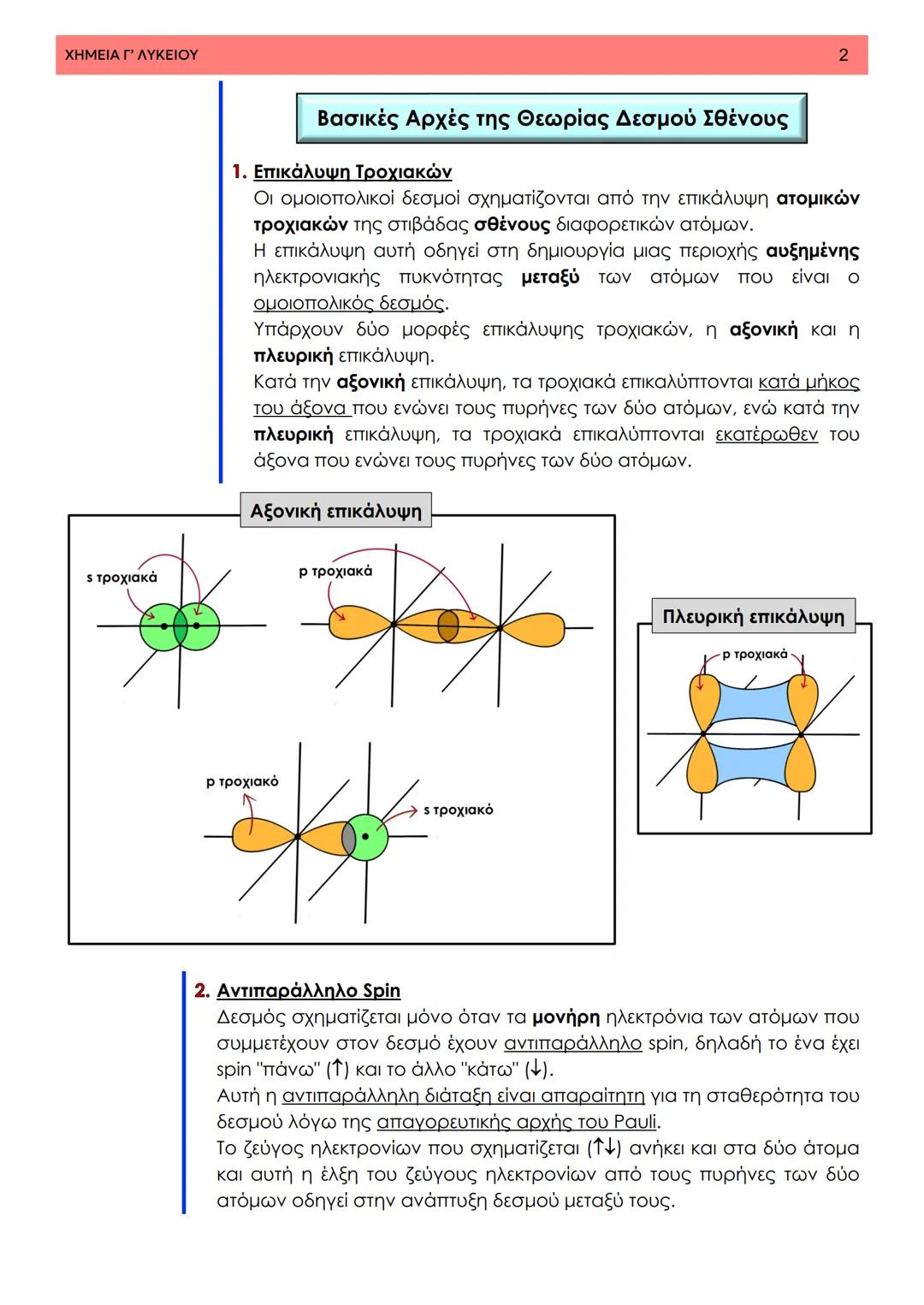
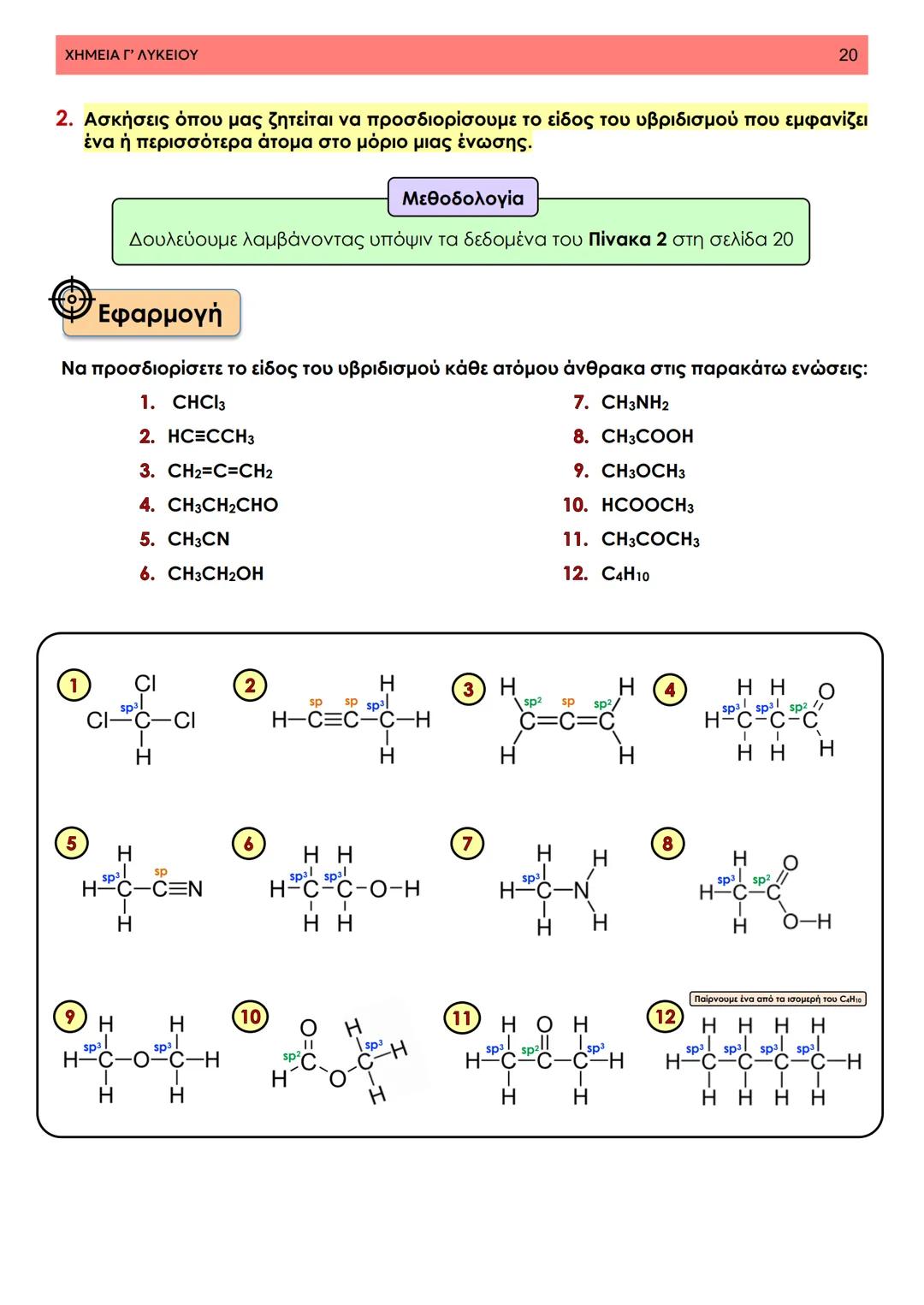
Οι σ δεσμοί έχουν κυλινδρική συμμετρία και η μέγιστη πυκνότητα του ηλεκτρονιακού νέφους βρίσκεται στον χώρο μεταξύ των δύο πυρήνων. Επιτρέπουν την περιστροφή γύρω από τον άξονα του δεσμού, κάτι που είναι κρίσιμο για τη μοριακή κινητικότητα.
Αντίθετα, οι π δεσμοί έχουν τη μέγιστη πυκνότητα ηλεκτρονιακού νέφους εκατέρωθεν του άξονα που συνδέει τους πυρήνες. Δεν επιτρέπουν περιστροφή, γεγονός που εξηγεί γιατί οι διπλοί δεσμοί είναι "στιφοί".
Τα s τροχιακά δεν μπορούν να συμμετέχουν σε πλευρικές επικαλύψεις λόγω της σφαιρικής τους συμμετρίας. Αυτός είναι ο λόγος που μόνο τα p τροχιακά σχηματίζουν π δεσμούς.
Προσοχή: Οι π δεσμοί είναι πάντα "συνοδευτικοί" - εμφανίζονται μαζί με σ δεσμούς στους διπλούς και τριπλούς δεσμούς.
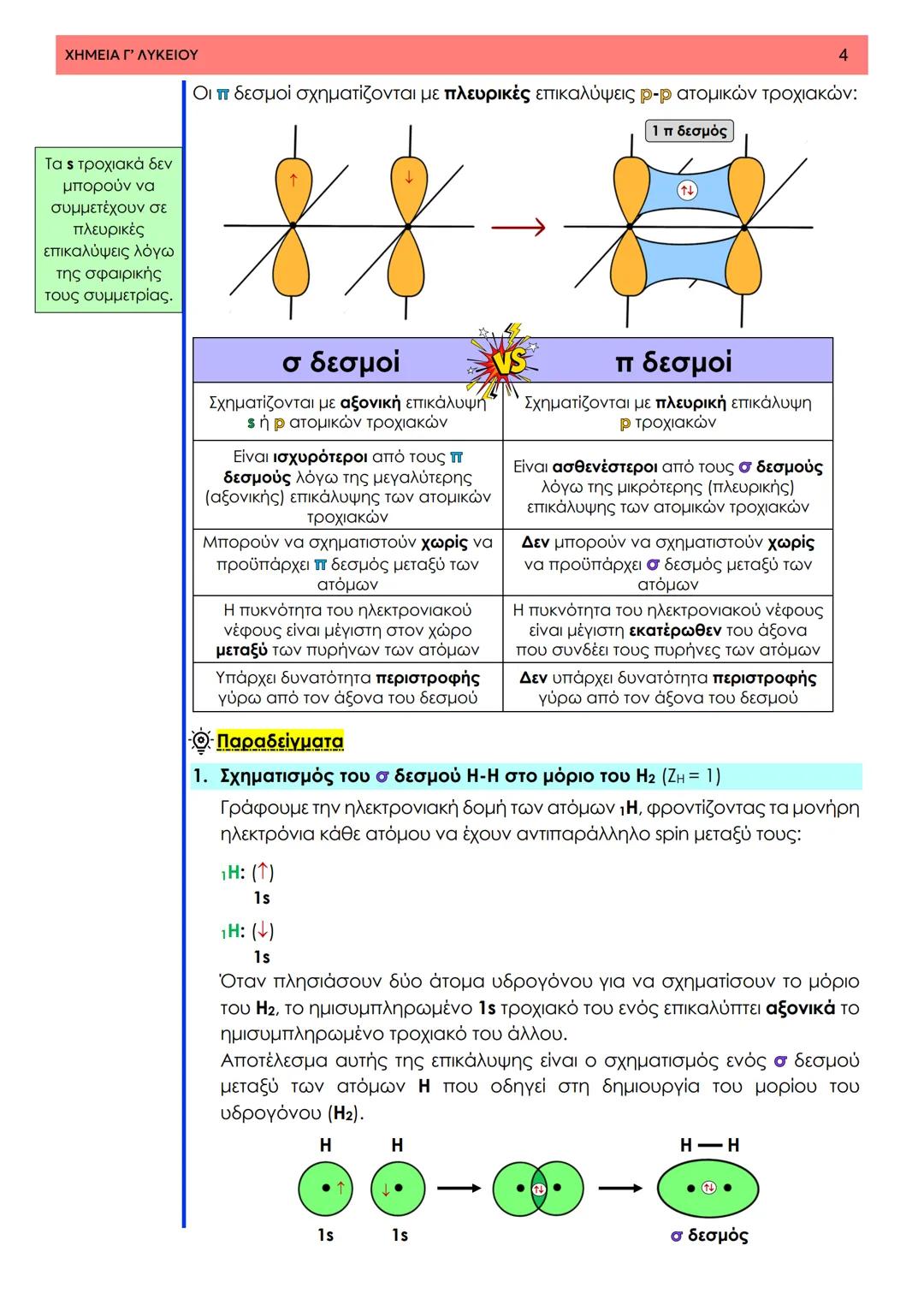
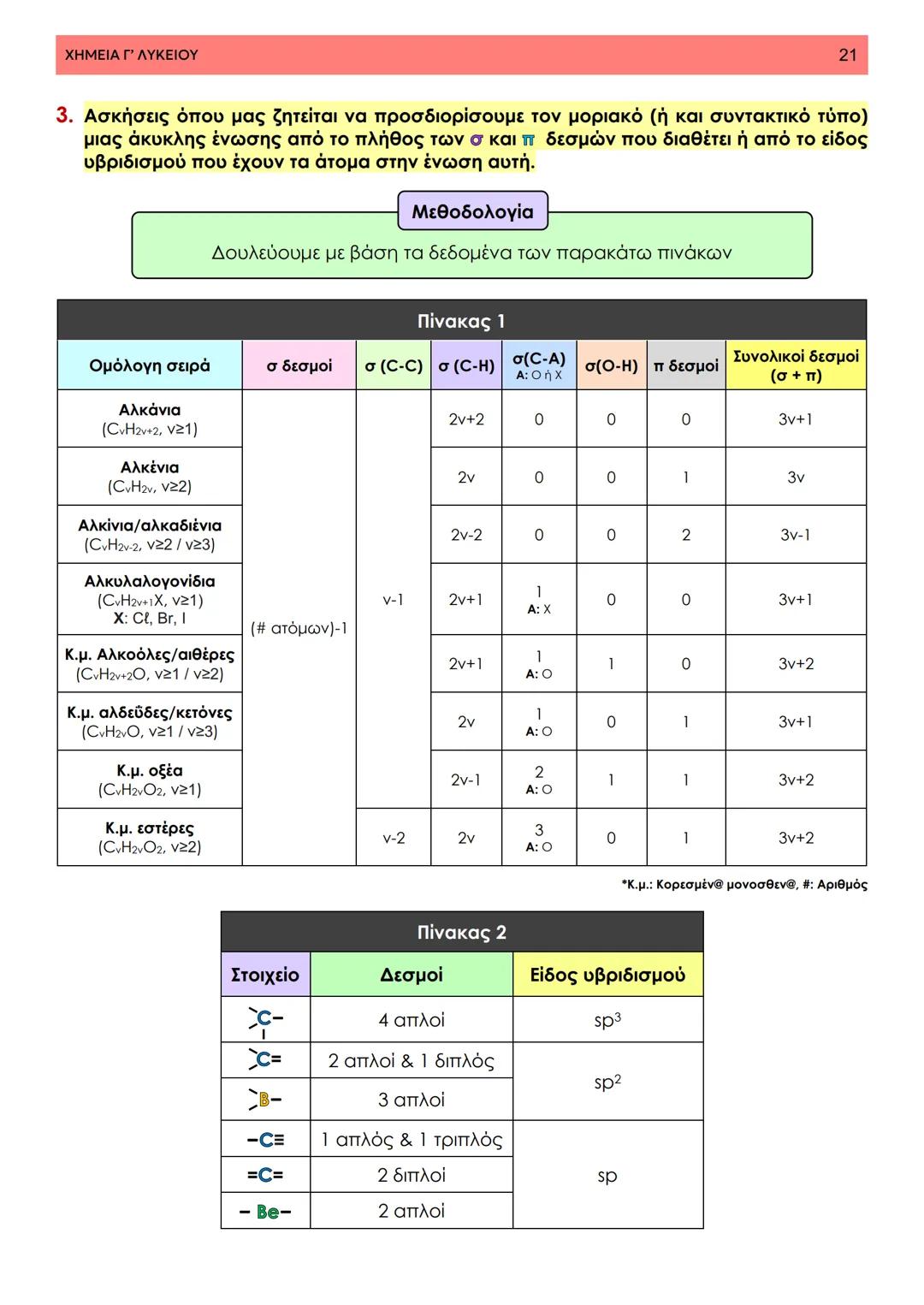
Στο μόριο του υδρογόνου (H₂), δύο άτομα H με αντιπαράλληλα spin επικαλύπτουν τα 1s τροχιακά τους αξονικά, δημιουργώντας έναν σ δεσμό. Το μήκος δεσμού είναι 0,74 Å και η ενέργεια δεσμού 436 kJ/mol.
Στο μόριο του φθορίου (F₂), τα ημισυμπληρωμένα 2p τροχιακά των δύο ατόμων επικαλύπτονται αξονικά, σχηματίζοντας έναν σ δεσμό. Στο μόριο του HF, το 1s του H επικαλύπτει το 2p του F.
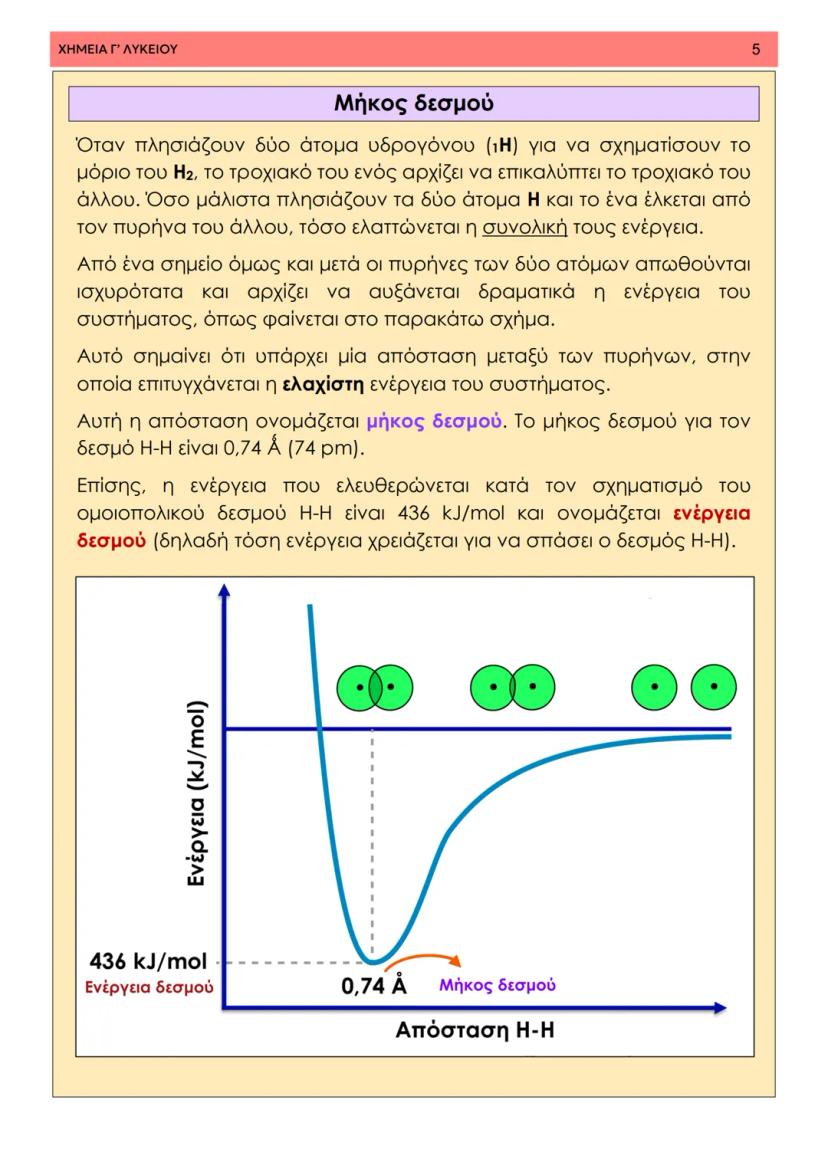
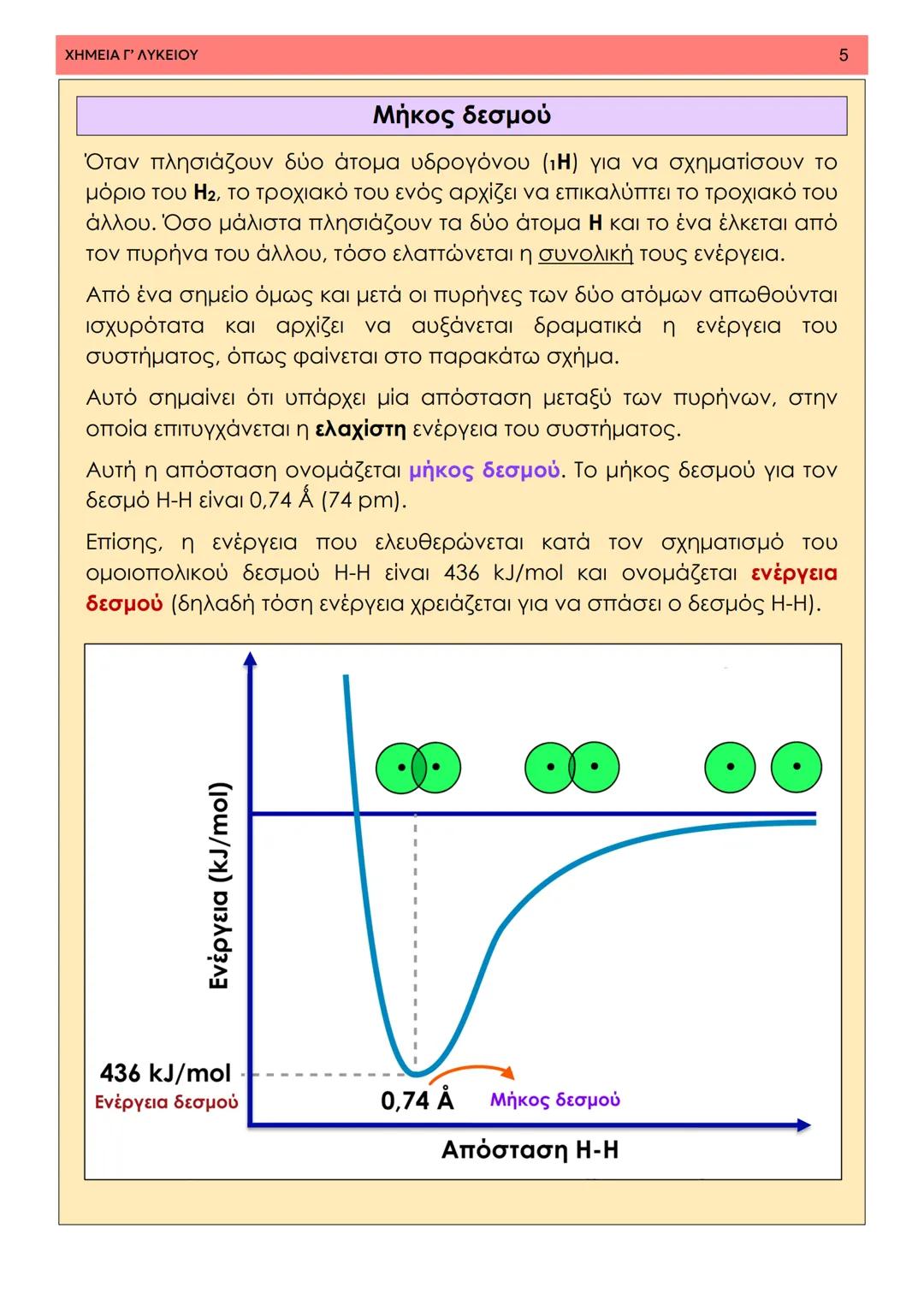
Όταν πλησιάζουν δύο άτομα, η ενέργεια του συστήματος μειώνεται αρχικά λόγω της έλξης. Ωστόσο, σε πολύ κοντινές αποστάσεις, οι πυρήνες απωθούνται ισχυρά, αυξάνοντας δραματικά την ενέργεια.
Σημείωση: Το μήκος δεσμού είναι η απόσταση στην οποία επιτυγχάνεται η ελάχιστη ενέργεια του συστήματος.
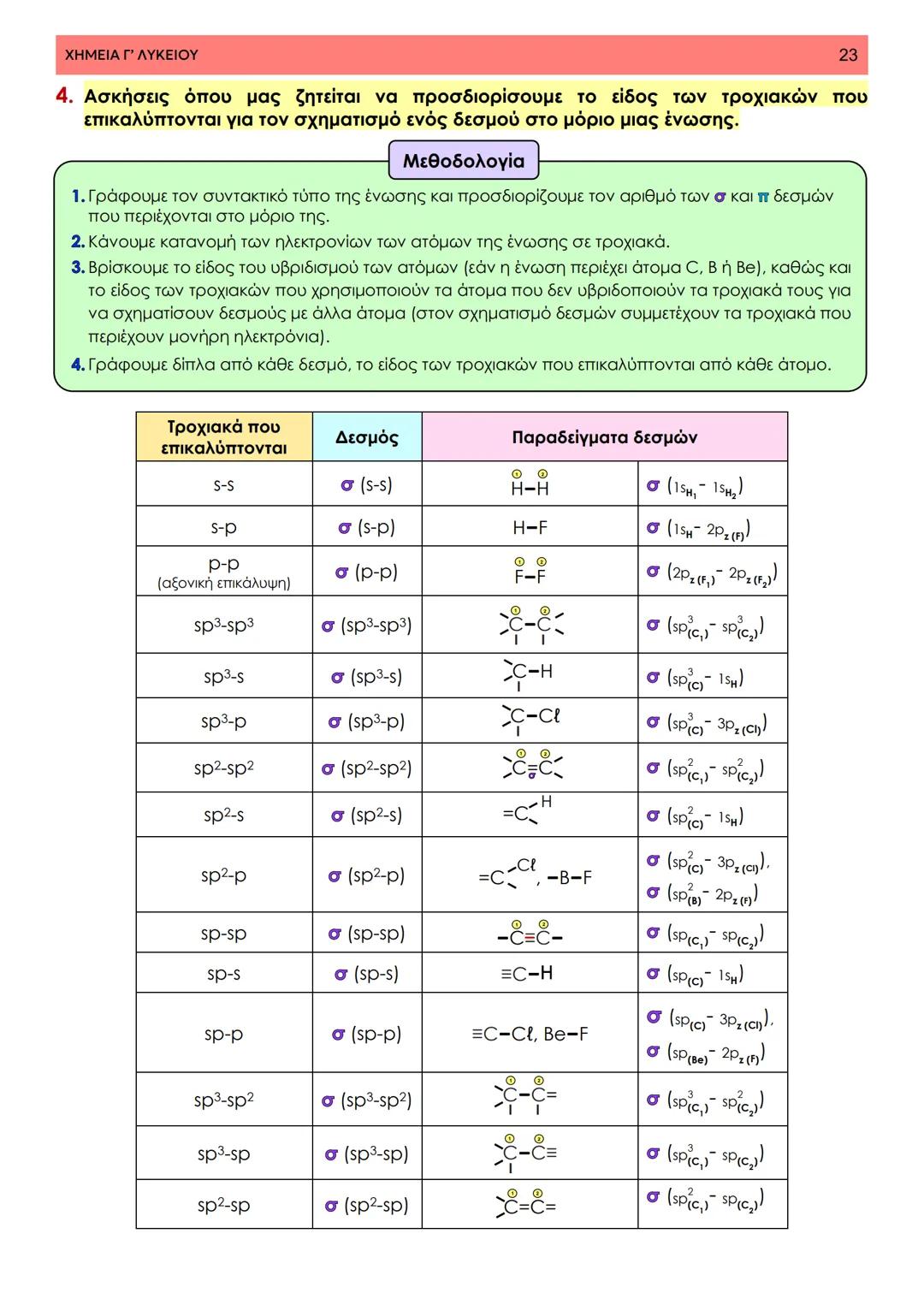
Όταν δύο άτομα πλησιάζουν για να σχηματίσουν δεσμό, η ενέργεια του συστήματος αρχικά μειώνεται καθώς τα ηλεκτρόνια έλκονται από τους πυρήνες και των δύο ατόμων. Αυτή η μείωση συνεχίζεται μέχρι ένα συγκεκριμένο σημείο.
Από εκεί και πέρα, οι πυρήνες των δύο ατόμων αρχίζουν να απωθούνται ισχυρότατα, προκαλώντας δραματική αύξηση της ενέργειας. Υπάρχει λοιπόν μία βέλτιστη απόσταση όπου η ενέργεια είναι ελάχιστη - αυτή ονομάζεται μήκος δεσμού.
Η ενέργεια που ελευθερώνεται κατά τον σχηματισμό του δεσμού ονομάζεται ενέργεια δεσμού. Για παράδειγμα, για τον δεσμό H-H είναι 436 kJ/mol - τόση ενέργεια χρειάζεται και για να τον σπάσουμε.
Πρακτική εφαρμογή: Αυτές οι έννοιες εξηγούν γιατί ορισμένες αντιδράσεις απελευθερώνουν ενέργεια ενώ άλλες τη χρειάζονται.
Στο μόριο του φθορίου (F₂), κάθε άτομο F έχει ένα μονήρες ηλεκτρόνιο στο 2pz τροχιακό. Όταν πλησιάσουν, αυτά τα τροχιακά επικαλύπτονται αξονικά και σχηματίζουν έναν σ δεσμό που κρατάει το μόριο μαζί.
Το μόριο του υδροφθορίου (HF) σχηματίζεται όταν το 1s τροχιακό του H (με ένα μονήρες ηλεκτρόνιο) επικαλύπτει αξονικά το ημισυμπληρωμένο 2pz τροχιακό του F. Και πάλι προκύπτει ένας σ δεσμός.
Σε όλες αυτές τις περιπτώσεις, τα μονήρη ηλεκτρόνια πρέπει να έχουν αντιπαράλληλο spin για να σχηματιστεί σταθερός δεσμός. Αυτή είναι μια θεμελιώδης απαίτηση της θεωρίας δεσμού σθένους.
Θυμηθείτε: Πάντα ελέγχετε ότι τα ηλεκτρόνια που συμμετέχουν στον δεσμό έχουν αντιπαράλληλα spin (↑↓).

Το μόριο του οξυγόνου (O₂) είναι ένα εξαιρετικό παράδειγμα για να κατανοήσετε τους διπλούς δεσμούς. Κάθε άτομο O έχει δύο μονήρη ηλεκτρόνια σε p τροχιακά, οπότε μπορεί να σχηματίσει δύο δεσμούς.
Αρχικά, ένα ημισυμπληρωμένο 2p τροχιακό του ενός ατόμου επικαλύπτει αξονικά το αντίστοιχο του άλλου, σχηματίζοντας έναν σ δεσμό. Στη συνέχεια, το δεύτερο μονήρες ηλεκτρόνιο κάθε ατόμου επικαλύπτει πλευρικά το αντίστοιχο του άλλου ατόμου, δημιουργώντας έναν π δεσμό.
Το αποτέλεσμα είναι ένας διπλός δεσμός που αποτελείται από έναν σ και έναν π δεσμό. Κάθε άτομο O διατηρεί επίσης δύο μη δεσμικά ζεύγη ηλεκτρονίων που δε συμμετέχουν στον δεσμό.
Σημαντικό: Σε κάθε πολλαπλό δεσμό, ο πρώτος είναι πάντα σ δεσμός και οι επόμενοι είναι π δεσμοί.

Το μόριο του αζώτου (N₂) σας δείχνει πώς λειτουργούν οι τριπλοί δεσμοί. Κάθε άτομο N έχει τρία μονήρη ηλεκτρόνια σε p τροχιακά, οπότε μπορεί να σχηματίσει τρεις δεσμούς με άλλο άτομο N.
Πρώτα σχηματίζεται ένας σ δεσμός από την αξονική επικάλυψη ενός ζεύγους p τροχιακών. Στη συνέχεια, τα υπόλοιπα δύο ζεύγη p τροχιακών επικαλύπτονται πλευρικά, δημιουργώντας δύο π δεσμούς.
Το αποτέλεσμα είναι ένας τριπλός δεσμός (N≡N) που αποτελείται από έναν σ δεσμό και δύο π δεσμούς. Αυτός είναι ένας από τους ισχυρότερους δεσμούς στη φύση, γι' αυτό το N₂ είναι τόσο σταθερό.
Κάθε άτομο N διατηρεί ένα μη δεσμικό ζεύγος ηλεκτρονίων στο 2s τροχιακό.
Προσοχή: Οι τριπλοί δεσμοί είναι πολύ ισχυροί αλλά και πολύ "στιφοί" - δεν επιτρέπουν περιστροφή λόγω των π δεσμών.

Όταν μελετήσουμε το μόριο του BeF₂, συναντάμε ένα πρόβλημα. Το Be στη θεμελιώδη κατάσταση έχει διαμόρφωση (↑↓)(↑↓) και δεν διαθέτει μονήρη ηλεκτρόνια για να σχηματίσει δεσμούς. Πώς λοιπόν σχηματίζεται το BeF₂;
Η λύση είναι ο υβριδισμός! Το Be προωθεί ένα ηλεκτρόνιο από το 2s στο 2p τροχιακό, δημιουργώντας δύο μονήρη ηλεκτρόνια. Όμως αυτό θα έδινε δύο διαφορετικούς τύπους δεσμών .
Πειραματικά όμως, οι δύο δεσμοί στο BeF₂ είναι ισότιμοι! Αυτό εξηγείται με τον υβριδισμό: τα s και p τροχιακά "ανασυνδυάζονται" και σχηματίζουν νέα υβριδικά τροχιακά με ίδια ενέργεια και σχήμα.
Κλειδί: Ο υβριδισμός εξηγεί πώς άτομα σχηματίζουν ισότιμους δεσμούς ακόμα και όταν χρησιμοποιούν διαφορετικά τροχιακά.






Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
App Store
Google Play
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
3Lithio
@3lithio
Η θεωρία δεσμού σθένους είναι μια από τις πιο σημαντικές κβαντομηχανικές θεωρίες που εξηγεί πώς σχηματίζονται οι ομοιοπολικοί δεσμοί στα μόρια. Αυτή η θεωρία, που διατυπώθηκε το 1931 από τους Pauling και Slater, θα σας βοηθήσει να καταλάβετε γιατί τα... Δες περισσότερα

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Στη θεωρία δεσμού σθένους, ο ομοιοπολικός δεσμός προκύπτει από την επικάλυψη ατομικών τροχιακών δύο ατόμων που περιέχουν μονήρη ηλεκτρόνια με αντιπαράλληλο spin. Φανταστείτε δύο άτομα που πλησιάζουν το ένα στο άλλο - τα τροχιακά τους επικαλύπτονται και δημιουργούν μια περιοχή αυξημένης ηλεκτρονιακής πυκνότητας.
Αυτή η επικάλυψη είναι που κρατάει τα άτομα μαζί, μειώνοντας την ενέργεια του συστήματος. Το αποτέλεσμα; Το μόριο γίνεται πιο σταθερό από τα μεμονωμένα άτομα.
Θυμηθείτε: Οι δεσμοί σχηματίζονται μόνο με ηλεκτρόνια που έχουν αντιπαράλληλο spin (↑↓), όπως ορίζει η απαγορευτική αρχή του Pauli.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Υπάρχουν δύο βασικοί τρόποι επικάλυψης τροχιακών. Η αξονική επικάλυψη γίνεται κατά μήκος του άξονα που ενώνει τους πυρήνες, ενώ η πλευρική επικάλυψη γίνεται εκατέρωθεν αυτού του άξονα.
Αυτοί οι τρόποι επικάλυψης δημιουργούν δύο διαφορετικούς τύπους δεσμών. Οι σ (σίγμα) δεσμοί προκύπτουν από αξονική επικάλυψη s-s, s-p ή p-p τροχιακών και είναι ισχυρότεροι. Οι π (πι) δεσμοί σχηματίζονται από πλευρική επικάλυψη p τροχιακών και είναι ασθενέστεροι.
Σημαντικό: Όσο μεγαλύτερη είναι η επικάλυψη των τροχιακών, τόσο ισχυρότερος είναι ο δεσμός που προκύπτει.
Οι π δεσμοί δεν μπορούν να υπάρξουν χωρίς να προϋπάρχει σ δεσμός μεταξύ των ίδιων ατόμων.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Οι σ δεσμοί έχουν κυλινδρική συμμετρία και η μέγιστη πυκνότητα του ηλεκτρονιακού νέφους βρίσκεται στον χώρο μεταξύ των δύο πυρήνων. Επιτρέπουν την περιστροφή γύρω από τον άξονα του δεσμού, κάτι που είναι κρίσιμο για τη μοριακή κινητικότητα.
Αντίθετα, οι π δεσμοί έχουν τη μέγιστη πυκνότητα ηλεκτρονιακού νέφους εκατέρωθεν του άξονα που συνδέει τους πυρήνες. Δεν επιτρέπουν περιστροφή, γεγονός που εξηγεί γιατί οι διπλοί δεσμοί είναι "στιφοί".
Τα s τροχιακά δεν μπορούν να συμμετέχουν σε πλευρικές επικαλύψεις λόγω της σφαιρικής τους συμμετρίας. Αυτός είναι ο λόγος που μόνο τα p τροχιακά σχηματίζουν π δεσμούς.
Προσοχή: Οι π δεσμοί είναι πάντα "συνοδευτικοί" - εμφανίζονται μαζί με σ δεσμούς στους διπλούς και τριπλούς δεσμούς.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Στο μόριο του υδρογόνου (H₂), δύο άτομα H με αντιπαράλληλα spin επικαλύπτουν τα 1s τροχιακά τους αξονικά, δημιουργώντας έναν σ δεσμό. Το μήκος δεσμού είναι 0,74 Å και η ενέργεια δεσμού 436 kJ/mol.
Στο μόριο του φθορίου (F₂), τα ημισυμπληρωμένα 2p τροχιακά των δύο ατόμων επικαλύπτονται αξονικά, σχηματίζοντας έναν σ δεσμό. Στο μόριο του HF, το 1s του H επικαλύπτει το 2p του F.
Όταν πλησιάζουν δύο άτομα, η ενέργεια του συστήματος μειώνεται αρχικά λόγω της έλξης. Ωστόσο, σε πολύ κοντινές αποστάσεις, οι πυρήνες απωθούνται ισχυρά, αυξάνοντας δραματικά την ενέργεια.
Σημείωση: Το μήκος δεσμού είναι η απόσταση στην οποία επιτυγχάνεται η ελάχιστη ενέργεια του συστήματος.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Όταν δύο άτομα πλησιάζουν για να σχηματίσουν δεσμό, η ενέργεια του συστήματος αρχικά μειώνεται καθώς τα ηλεκτρόνια έλκονται από τους πυρήνες και των δύο ατόμων. Αυτή η μείωση συνεχίζεται μέχρι ένα συγκεκριμένο σημείο.
Από εκεί και πέρα, οι πυρήνες των δύο ατόμων αρχίζουν να απωθούνται ισχυρότατα, προκαλώντας δραματική αύξηση της ενέργειας. Υπάρχει λοιπόν μία βέλτιστη απόσταση όπου η ενέργεια είναι ελάχιστη - αυτή ονομάζεται μήκος δεσμού.
Η ενέργεια που ελευθερώνεται κατά τον σχηματισμό του δεσμού ονομάζεται ενέργεια δεσμού. Για παράδειγμα, για τον δεσμό H-H είναι 436 kJ/mol - τόση ενέργεια χρειάζεται και για να τον σπάσουμε.
Πρακτική εφαρμογή: Αυτές οι έννοιες εξηγούν γιατί ορισμένες αντιδράσεις απελευθερώνουν ενέργεια ενώ άλλες τη χρειάζονται.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Στο μόριο του φθορίου (F₂), κάθε άτομο F έχει ένα μονήρες ηλεκτρόνιο στο 2pz τροχιακό. Όταν πλησιάσουν, αυτά τα τροχιακά επικαλύπτονται αξονικά και σχηματίζουν έναν σ δεσμό που κρατάει το μόριο μαζί.
Το μόριο του υδροφθορίου (HF) σχηματίζεται όταν το 1s τροχιακό του H (με ένα μονήρες ηλεκτρόνιο) επικαλύπτει αξονικά το ημισυμπληρωμένο 2pz τροχιακό του F. Και πάλι προκύπτει ένας σ δεσμός.
Σε όλες αυτές τις περιπτώσεις, τα μονήρη ηλεκτρόνια πρέπει να έχουν αντιπαράλληλο spin για να σχηματιστεί σταθερός δεσμός. Αυτή είναι μια θεμελιώδης απαίτηση της θεωρίας δεσμού σθένους.
Θυμηθείτε: Πάντα ελέγχετε ότι τα ηλεκτρόνια που συμμετέχουν στον δεσμό έχουν αντιπαράλληλα spin (↑↓).

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Το μόριο του οξυγόνου (O₂) είναι ένα εξαιρετικό παράδειγμα για να κατανοήσετε τους διπλούς δεσμούς. Κάθε άτομο O έχει δύο μονήρη ηλεκτρόνια σε p τροχιακά, οπότε μπορεί να σχηματίσει δύο δεσμούς.
Αρχικά, ένα ημισυμπληρωμένο 2p τροχιακό του ενός ατόμου επικαλύπτει αξονικά το αντίστοιχο του άλλου, σχηματίζοντας έναν σ δεσμό. Στη συνέχεια, το δεύτερο μονήρες ηλεκτρόνιο κάθε ατόμου επικαλύπτει πλευρικά το αντίστοιχο του άλλου ατόμου, δημιουργώντας έναν π δεσμό.
Το αποτέλεσμα είναι ένας διπλός δεσμός που αποτελείται από έναν σ και έναν π δεσμό. Κάθε άτομο O διατηρεί επίσης δύο μη δεσμικά ζεύγη ηλεκτρονίων που δε συμμετέχουν στον δεσμό.
Σημαντικό: Σε κάθε πολλαπλό δεσμό, ο πρώτος είναι πάντα σ δεσμός και οι επόμενοι είναι π δεσμοί.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Το μόριο του αζώτου (N₂) σας δείχνει πώς λειτουργούν οι τριπλοί δεσμοί. Κάθε άτομο N έχει τρία μονήρη ηλεκτρόνια σε p τροχιακά, οπότε μπορεί να σχηματίσει τρεις δεσμούς με άλλο άτομο N.
Πρώτα σχηματίζεται ένας σ δεσμός από την αξονική επικάλυψη ενός ζεύγους p τροχιακών. Στη συνέχεια, τα υπόλοιπα δύο ζεύγη p τροχιακών επικαλύπτονται πλευρικά, δημιουργώντας δύο π δεσμούς.
Το αποτέλεσμα είναι ένας τριπλός δεσμός (N≡N) που αποτελείται από έναν σ δεσμό και δύο π δεσμούς. Αυτός είναι ένας από τους ισχυρότερους δεσμούς στη φύση, γι' αυτό το N₂ είναι τόσο σταθερό.
Κάθε άτομο N διατηρεί ένα μη δεσμικό ζεύγος ηλεκτρονίων στο 2s τροχιακό.
Προσοχή: Οι τριπλοί δεσμοί είναι πολύ ισχυροί αλλά και πολύ "στιφοί" - δεν επιτρέπουν περιστροφή λόγω των π δεσμών.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Όταν μελετήσουμε το μόριο του BeF₂, συναντάμε ένα πρόβλημα. Το Be στη θεμελιώδη κατάσταση έχει διαμόρφωση (↑↓)(↑↓) και δεν διαθέτει μονήρη ηλεκτρόνια για να σχηματίσει δεσμούς. Πώς λοιπόν σχηματίζεται το BeF₂;
Η λύση είναι ο υβριδισμός! Το Be προωθεί ένα ηλεκτρόνιο από το 2s στο 2p τροχιακό, δημιουργώντας δύο μονήρη ηλεκτρόνια. Όμως αυτό θα έδινε δύο διαφορετικούς τύπους δεσμών .
Πειραματικά όμως, οι δύο δεσμοί στο BeF₂ είναι ισότιμοι! Αυτό εξηγείται με τον υβριδισμό: τα s και p τροχιακά "ανασυνδυάζονται" και σχηματίζουν νέα υβριδικά τροχιακά με ίδια ενέργεια και σχήμα.
Κλειδί: Ο υβριδισμός εξηγεί πώς άτομα σχηματίζουν ισότιμους δεσμούς ακόμα και όταν χρησιμοποιούν διαφορετικά τροχιακά.

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές

Πρόσβαση σε όλα τα έγγραφα
Βελτίωσε τους βαθμούς σου
Γίνε μέλος με εκατομμύρια μαθητές
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
6
Έξυπνα Εργαλεία ΝΕΟ
Μετέτρεψε αυτές τις σημειώσεις σε: ✓ 50+ Ερωτήσεις Εξάσκησης ✓ Διαδραστικές Κάρτες Μνήμης ✓ Πλήρες Προσομοιωτικό Διαγώνισμα ✓ Σχέδια Δοκιμίου
App Store
Google Play
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Στέφαν Σ
χρήστης iOS
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Σαμάνθα Κλιχ
χρήστης Android
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Άννα
χρήστης iOS
Το Knowunity είναι ότι πρέπει Για μαθητές οι οποίοι όντως έχουν την θέληση για μάθηση καθώς δεν είναι σαν τις άλλες εφαρμογές που σου δίνουν απευθείας την λύση όμως σου εξηγούν λεπτομερώς και την σημασία – νόημα αυτού του οποίου ψάχνεις ! Καταπληκτική εφεύρεση ! Ένας από τους λόγους για τον οποίο χαίρομαι που Η τεχνητή νοημοσύνη εξελίσσεται .
Φασαια
χρήστης iOS
τέλειοοο
Λίζα Μ
χρήστης Android
Αυτή η εφαρμογή με έχει κάνει τα θέλω να διαβάζω με βοηθάει πάρα πολύ
Καμαρινός Γ
χρήστης iOS
Η εφαρμογή είναι τέλεια! Το μόνο που χρειάζεται να κάνω είναι να εισάγω το θέμα στη γραμμή αναζήτησης και παίρνω την απάντηση πολύ γρήγορα. Δεν χρειάζεται να παρακολουθήσω 10 βίντεο στο YouTube για να καταλάβω κάτι, άρα εξοικονομώ χρόνο. Τη συνιστώ ανεπιφύλακτα!
Sudenaz Ocak
χρήστης Android
Στο σχολείο ήμουν πολύ κακός στα μαθηματικά, αλλά χάρη στην εφαρμογή τα πάω καλύτερα τώρα. Είμαι τόσο ευγνώμων που δημιούργησες την εφαρμογή.
Greenlight Bonnie
χρήστης Android
Το καλύτερο που υπάρχει αυτό έχω να πω εγώ
Τζούλια Σ
χρήστης Android
με βοηθάει πάρα πολύ στα μαθήματα πρέπει να το κατεβάσετε είναι ότι καλύτερο
Αγγο
χρήστης iOS
ΤΑ ΚΟΥΙΖ ΚΑΙ ΟΙ ΚΑΡΤΕΣ ΜΝΗΜΗΣ ΕΙΝΑΙ ΤΟΣΟ ΧΡΗΣΙΜΑ ΚΑΙ ΛΑΤΡΕΥΩ ΤΟ Knowunity ΤΝ. ΕΙΝΑΙ ΚΥΡΙΟΛΕΚΤΙΚΑ ΣΑΝ ΤΟ CHATGPT ΑΛΛΑ ΠΙΟ ΕΞΥΠΝΟ!! ΜΕ ΒΟΗΘΗΣΕ ΚΑΙ ΜΕ TA ΠΡΟΒΛΗΜΑΤΑ ΜΕ ΤΗ ΜΑΣΚΑΡΑ ΜΟΥ!! ΚΑΘΩΣ ΚΑΙ ΜΕ ΤΑ ΚΑΝΟΝΙΚΑ ΜΟΥ ΜΑΘΗΜΑΤΑ! ΞΕΚΑΘΑΡΑ 😍😁😲🤑💗✨🎀😮
Μαριλου
χρήστης Android
Η εφαρμογή αυτή είναι τέλεια Αν έχεις κάποια κενά ή κάποιος καθηγητής/καθηγητριά σου (ιδιαίτερα αν πας σε δημόσιο ) δεν κάνει καλό μάθημα ή δεν μπορείς να καταλάβεις το so σε βοηθάει με ερωτήσεις και μπορείς να βρεις πολλές σημειώσεις σε μαθήματα από άλλους μαθητές. Εγώ που δυσκολεύομαι με κάποια μαθήματα αυτή η εφαρμογή με έχει βοηθήσει να τα κατανοήσω όσο καλύτερα μπορώ
Thenia
χρήστης iOS