Ετοιμάσου να εξερευνήσεις τον συναρπαστικό κόσμο της χημείας! Σε αυτές... Δες περισσότερα
Χημεία Α’ Λυκείου: Πλήρεις Σημειώσεις












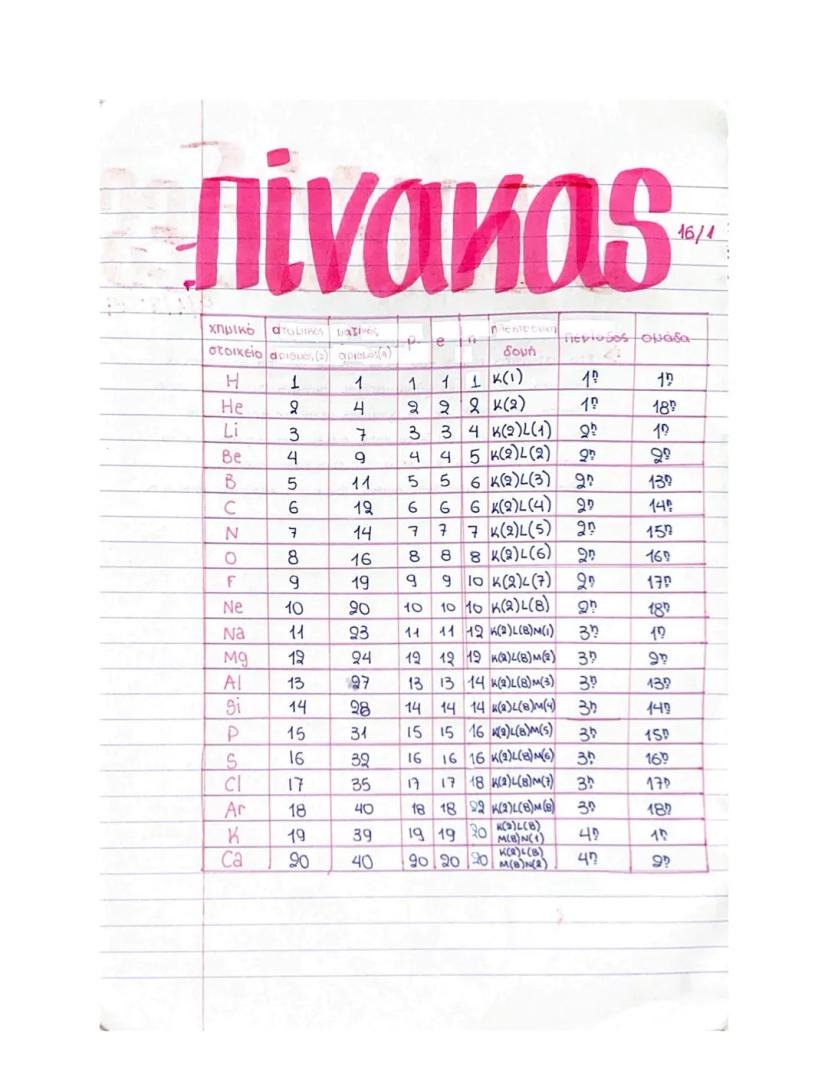















Το πυρηνικό άτομο
Το άτομο αποτελείται από τον πυρήνα, που περιέχει πρωτόνια (με θετικό φορτίο) και νετρόνια (χωρίς φορτίο). Γύρω από τον πυρήνα περιφέρονται τα ηλεκτρόνια.
Κάθε άτομο χαρακτηρίζεται από δύο βασικούς αριθμούς:
- Ο ατομικός αριθμός (Ζ) δείχνει τον αριθμό των πρωτονίων στον πυρήνα και καθορίζει τη χημική ταυτότητα του στοιχείου
- Ο μαζικός αριθμός (Α) είναι το σύνολο πρωτονίων και νετρονίων στον πυρήνα
Τα ισότοπα είναι άτομα του ίδιου στοιχείου (ίδιο Ζ) αλλά με διαφορετικό αριθμό νετρονίων (διαφορετικό Α). Για παράδειγμα:
- Νάτριο (Na): Z=11, A=23 → 11 πρωτόνια, 12 νετρόνια
- Ασβέστιο (Ca): Z=20, A=40 → 20 πρωτόνια, 20 νετρόνια
Σημαντικό! Το χημικό σύμβολο κάθε στοιχείου γράφεται με το μαζικό αριθμό πάνω αριστερά και τον ατομικό αριθμό κάτω αριστερά π.χ. $^{23}_{11}Na$.

Η μονάδα mol
Το mol είναι η βασική μονάδα ποσότητας ουσίας στο Διεθνές Σύστημα Μονάδων (SI). Ένα mol περιέχει ακριβώς 6,02×10²³ οντότητες (άτομα, μόρια ή ιόντα) - αυτός ο αριθμός ονομάζεται αριθμός Avogadro (N₀).
Ένα mol ατόμων ή μορίων έχει μάζα σε γραμμάρια ίση με την ατομική ή μοριακή μάζα αντίστοιχα. Έτσι:
- 1 mol ατόμων περιέχει N₀ άτομα και ζυγίζει Ar g
- 1 mol μορίων περιέχει N₀ μόρια και ζυγίζει Mr g
Για παράδειγμα, σε ένα μόριο H₂SO₄ υπάρχουν:
- 2 άτομα υδρογόνου (H)
- 1 άτομο θείου (S)
- 4 άτομα οξυγόνου (O)
Αντίστοιχα, σε 1 mol H₂SO₄ έχουμε:
- 2 mol ατόμων H (2N₀ άτομα)
- 1 mol ατόμων S (N₀ άτομα)
- 4 mol ατόμων O (4N₀ άτομα)
Απλοποίηση: Σκέψου το mol ως ένα "πακέτο" ατόμων ή μορίων που περιέχει πάντα τον ίδιο αριθμό σωματιδίων, όπως ένα πακέτο αναψυκτικών περιέχει πάντα 6 κουτάκια.

Μετατροπές μάζας και mol
Η σχέση μεταξύ μάζας (m) μιας ουσίας και του αριθμού mol (n) είναι θεμελιώδης στη χημεία. Χρησιμοποιούμε τη μοριακή μάζα (Mr) για τις μετατροπές αυτές.
Για να βρούμε τον αριθμό mol από τη μάζα: n = m / Mr
Για να βρούμε τη μάζα από τον αριθμό mol: m = n · Mr
Παραδείγματα:
-
Πόσο ζυγίζουν 5 mol νερού (H₂O); Mr(H₂O) = 18 g/mol, άρα m = 5 mol · 18 g/mol = 90 g
-
Πόσο ζυγίζουν 5 mol νατρίου (Na); Mr(Na) = 23 g/mol, άρα m = 5 mol · 23 g/mol = 115 g
-
Πόσο ζυγίζουν 5 mol θειικού οξέος (H₂SO₄); Mr(H₂SO₄) = 98 g/mol, άρα m = 5 mol · 98 g/mol = 490 g
-
Πόσα mol είναι 85 g αμμωνίας (NH₃); Mr(NH₃) = 17 g/mol, άρα n = 85 g / 17 g/mol = 5 mol
Συμβουλή: Σε ασκήσεις χημείας, πάντα ξεκινάμε με τον υπολογισμό της μοριακής μάζας (Mr) των ενώσεων που εμφανίζονται στο πρόβλημα.

Μονάδες συγκέντρωσης διαλυμάτων
Η συγκέντρωση (C) ή molarity (M) ενός διαλύματος δείχνει πόσα mol διαλυμένης ουσίας περιέχονται σε 1 λίτρο (L) διαλύματος:
C = n / V
Από αυτό τον τύπο μπορούμε να υπολογίσουμε:
- Τον αριθμό mol: n = C · V
- Τον όγκο του διαλύματος: V = n / C
- Τη μάζα της διαλυμένης ουσίας: m = n · Mr = C · V · Mr
Παραδείγματα:
-
Πόσα mol H₂SO₄ περιέχονται σε 5L διαλύματος H₂SO₄ 1,9M; n = C · V = 1,9 mol/L · 5L = 9,5 mol
-
Σε πόσα λίτρα διαλύματος H₂SO₄ 1,9M περιέχονται 6 mol H₂SO₄; V = n / C = 6 mol / 1,9 mol/L = 3,15 L
-
Σε 5L διαλύματος H₂SO₄ περιέχονται 588g H₂SO₄. Ποια είναι η συγκέντρωση; Mr(H₂SO₄) = 98 g/mol n = m / Mr = 588g / 98 g/mol = 6 mol C = n / V = 6 mol / 5L = 1,2M
Πρακτική συμβουλή: Στις εξετάσεις, οι ασκήσεις με συγκεντρώσεις απαιτούν προσοχή στις μονάδες. Πάντα μετατρέπουμε τον όγκο σε λίτρα (L) πριν εφαρμόσουμε τους τύπους!

Αραίωση διαλυμάτων
Κατά την αραίωση ενός διαλύματος, προσθέτουμε διαλύτη (συνήθως νερό) χωρίς να αλλάζει η ποσότητα της διαλυμένης ουσίας. Έτσι, ο αριθμός mol παραμένει σταθερός:
n₁ = n₂ ή C₁·V₁ = C₂·V₂
Όπου:
- C₁, V₁: η αρχική συγκέντρωση και ο αρχικός όγκος
- C₂, V₂: η τελική συγκέντρωση και ο τελικός όγκος
Για παράδειγμα, αν 20mL διαλύματος H₂SO₄ 5M αραιωθούν με προσθήκη 70mL H₂O, η συγκέντρωση του αραιωμένου διαλύματος θα είναι:
- C₁ = 5M
- V₁ = 20mL = 0,020L
- V₂ = V₁ + VH₂O = 20mL + 70mL = 90mL = 0,090L
- C₂ = C₁·V₁/V₂ = 5M·0,020L/0,090L = 1,1M
Ο τύπος C₁·V₁ = C₂·V₂ είναι θεμελιώδης για προβλήματα αραίωσης και χρησιμοποιείται συχνά στο εργαστήριο και στις εξετάσεις.
Θυμήσου: Στην αραίωση ο αριθμός των mol της διαλυμένης ουσίας παραμένει σταθερός, αλλά μοιράζεται σε μεγαλύτερο όγκο, με αποτέλεσμα η συγκέντρωση να μειώνεται.

Διαλυτότητα
Διαλυτότητα είναι η μέγιστη ποσότητα μιας ουσίας που μπορεί να διαλυθεί σε ορισμένη ποσότητα διαλύτη, υπό συγκεκριμένες συνθήκες θερμοκρασίας και πίεσης. Ουσιαστικά, εκφράζει την περιεκτικότητα ενός κορεσμένου διαλύματος.
Τα διαλύματα χαρακτηρίζονται ως:
- Κορεσμένα: περιέχουν τη μέγιστη ποσότητα διαλυμένης ουσίας
- Ακόρεστα: περιέχουν μικρότερη ποσότητα διαλυμένης ουσίας από τη μέγιστη δυνατή
Η διαλυτότητα επηρεάζεται από:
-
Τη φύση του διαλύτη: Ισχύει ο κανόνας "τα όμοια διαλύουν όμοια". Διαλύτης και διαλυμένη ουσία πρέπει να έχουν παρόμοια χημική δομή.
-
Τη θερμοκρασία:
- Για τα στερεά: η διαλυτότητά τους στο νερό αυξάνεται με την αύξηση της θερμοκρασίας
- Για τα αέρια: η διαλυτότητά τους στο νερό μειώνεται με την αύξηση της θερμοκρασίας
-
Την πίεση: Η διαλυτότητα των αερίων στο νερό αυξάνεται με την αύξηση της πίεσης.
Καθημερινή εφαρμογή: Γι' αυτό τα αναψυκτικά χάνουν το ανθρακικό τους (CO₂) όταν ζεσταίνονται ή όταν ανοίγουμε το μπουκάλι (μείωση πίεσης)!

Ηλεκτρονικές στοιβάδες
Στο ατομικό μοντέλο του Bohr, τα ηλεκτρόνια κινούνται σε καθορισμένες τροχιές (στοιβάδες) γύρω από τον πυρήνα. Κάθε στοιβάδα έχει συγκεκριμένη ενέργεια και χωρητικότητα ηλεκτρονίων.
Για τα γνωστά χημικά στοιχεία υπάρχουν επτά στοιβάδες, που ονομάζονται με τα λατινικά γράμματα K, L, M, N, O, P, Q. Κάθε στοιβάδα χαρακτηρίζεται από τον κύριο κβαντικό αριθμό n.
Η κατανομή των ηλεκτρονίων στις στοιβάδες καθορίζει τις χημικές ιδιότητες του ατόμου. Ιδιαίτερα σημαντικά είναι τα ηλεκτρόνια της εξωτερικής στοιβάδας (ηλεκτρόνια σθένους), που καθορίζουν τη χημική συμπεριφορά του ατόμου.
Η πλήρωση των στοιβάδων γίνεται προοδευτικά από τις εσωτερικές προς τις εξωτερικές, και κάθε στοιβάδα έχει μέγιστη χωρητικότητα 2n² ηλεκτρόνια, όπου n είναι ο κύριος κβαντικός αριθμός.
Χρήσιμο για το σχολείο: Τα στοιχεία με ίδιο αριθμό ηλεκτρονίων στην εξωτερική τους στοιβάδα ανήκουν στην ίδια ομάδα του Περιοδικού Πίνακα και έχουν παρόμοιες χημικές ιδιότητες!

Περιοδικός Πίνακας Στοιχείων
Ο Περιοδικός Πίνακας οργανώνει τα χημικά στοιχεία με βάση τον ατομικό τους αριθμό (Ζ) σε περιόδους (οριζόντιες σειρές) και ομάδες (κατακόρυφες στήλες).
Μερικά βασικά στοιχεία και οι ιδιότητές τους:
- Υδρογόνο (H): Z=1, περίοδος 1, ομάδα 1Α
- Ήλιο (He): Z=2, περίοδος 1, ομάδα 18Α (ευγενές αέριο)
- Λίθιο (Li): Z=3, περίοδος 2, ομάδα 1Α (αλκάλιο)
- Άνθρακας (C): Z=6, περίοδος 2, ομάδα 14Α
- Οξυγόνο (O): Z=8, περίοδος 2, ομάδα 16Α
- Νάτριο (Na): Z=11, περίοδος 3, ομάδα 1Α (αλκάλιο)
- Χλώριο (Cl): Z=17, περίοδος 3, ομάδα 17Α (αλογόνο)
Τα στοιχεία της ίδιας ομάδας έχουν παρόμοιες ιδιότητες επειδή έχουν τον ίδιο αριθμό ηλεκτρονίων στην εξωτερική τους στοιβάδα. Για παράδειγμα, τα αλκάλια (ομάδα 1Α) έχουν 1 ηλεκτρόνιο στην εξωτερική στοιβάδα και είναι πολύ δραστικά μέταλλα.
Έξυπνο κόλπο: Ο αριθμός της ομάδας (για τις κύριες ομάδες) συχνά αντιστοιχεί στον αριθμό των ηλεκτρονίων της εξωτερικής στοιβάδας!

Ατομική ακτίνα και περιοδικότητα
Η χημική συμπεριφορά των ατόμων καθορίζεται κυρίως από:
-
Τα ηλεκτρόνια της εξωτερικής στοιβάδας, που συμμετέχουν στους χημικούς δεσμούς.
-
Την ατομική ακτίνα: Όσο μεγαλύτερη είναι η ατομική ακτίνα, τόσο μικρότερη είναι η ελκτική δύναμη του πυρήνα στα εξωτερικά ηλεκτρόνια. Έτσι, τα μεγαλύτερα άτομα αποβάλλουν ευκολότερα ηλεκτρόνια.
Στοιχεία με παρόμοιες χημικές ιδιότητες έχουν παρόμοια ηλεκτρονική δομή στην εξωτερική στοιβάδα. Για παράδειγμα, το Li⁺ και το Na⁺ έχουν παρόμοιες ιδιότητες.
Μεταβολή της ατομικής ακτίνας:
-
Κατά μήκος μιας περιόδου (από αριστερά προς τα δεξιά): Η ατομική ακτίνα μειώνεται, καθώς αυξάνονται τα πρωτόνια και οι ελκτικές δυνάμεις προς τα εξωτερικά ηλεκτρόνια.
-
Κατά μήκος μιας ομάδας (από πάνω προς τα κάτω): Η ατομική ακτίνα αυξάνεται, καθώς αυξάνεται ο αριθμός των στοιβάδων και η απόσταση των εξωτερικών ηλεκτρονίων από τον πυρήνα.
Σημείωση: Όσο μεγαλύτερο είναι ένα άτομο, τόσο πιο αργά κινούνται τα ηλεκτρόνιά του και τόσο ευκολότερα τα αποβάλλει (αν είναι μέταλλο)!

Περιοδικές ιδιότητες και μεγέθη ατόμων
Η μεταβολή της ατομικής ακτίνας στον περιοδικό πίνακα ακολουθεί συγκεκριμένα μοτίβα που μας βοηθούν να κατανοήσουμε και να προβλέψουμε τη χημική συμπεριφορά των στοιχείων.
Κατά μήκος μιας περιόδου (από αριστερά προς τα δεξιά):
- Η ατομική ακτίνα μειώνεται
- Ο ατομικός αριθμός αυξάνεται, προσθέτοντας πρωτόνια στον πυρήνα
- Η ελκτική δύναμη του πυρήνα προς τα ηλεκτρόνια σθένους αυξάνεται
- Τα ηλεκτρόνια έλκονται πιο κοντά στον πυρήνα, μειώνοντας το μέγεθος του ατόμου
Κατά μήκος μιας ομάδας (από πάνω προς τα κάτω):
- Η ατομική ακτίνα αυξάνεται
- Ο αριθμός των ηλεκτρονικών στοιβάδων αυξάνεται
- Η απόσταση της εξωτερικής στοιβάδας από τον πυρήνα μεγαλώνει
- Η ελκτική δύναμη του πυρήνα μειώνεται λόγω της απόστασης
- Το άτομο γίνεται μεγαλύτερο
Πρακτική σημασία: Αυτή η γνώση μας βοηθά να προβλέψουμε τη δραστικότητα των μετάλλων. Για παράδειγμα, το κάλιο (K) είναι πιο δραστικό από το νάτριο (Na) επειδή έχει μεγαλύτερη ατομική ακτίνα και αποβάλλει ευκολότερα το εξωτερικό του ηλεκτρόνιο.

















Νομίζαμε ότι δε θα ρωτούσες ποτέ...
Τι είναι ο AI σύντροφος του Knowunity;
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Πού μπορώ να κατεβάσω την εφαρμογή Knowunity;
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Πώς μπορώ να λάβω την πληρωμή μου; Πόσα μπορώ να κερδίσω;
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
Πιο δημοφιλή περιεχόμενα στο Χημεία
9Οργανική χημεία
Όλες οι αντιδράσεις ανά κατηγορία.
Ονοματολογία κυριων στοιχείων
Χημεια α λυκειου
χημεια γ λυκειου
Έλεγχος γνώσεων στην χημεία της Γ' Λυκείου. Εξετάζονται θέματα οργανικής χημείας, αντιδράσεων και ενώσεων.
Ονοματολογία
Χημεία Α λυκείου
Χημεία α λυκείου
1ο ,2ο ,3ο κεφάλαιο χημείας α λυκείου
χημική ισορροπία
όλο το κεφάλαιο
χημική κινητική
όλες οι σημειώσεις του κεφαλαίου
Διαμοριακές δυνάμεις Χημεία Γ' λυκείου
Σημειωσεις στο κεφάλαιο των διαμοριακών δυνάμεων της χημειας γ λυκειου
Θερμοχημεία - Ενθαλπία
Επεξήγηση, περιληπτική, του κεφαλαίου της Θερμοχημειας στην ύλη της Γ´ Λυκείου.
Πιο δημοφιλή περιεχόμενα
9Ιστορια β λυκειου ολοι οι ορισμοι τις τραπεζας
Ορισμοί ιστόριας
Σχεδιαγράμματα όλης της ύλης ιστορίας α λυκείου
Σας έχω σχεδιαγράμματα όλης της εξεταστέας ύλης της α λυκείου για να διευκολυνθείτε από το τεράστιο βάρος του βιβλίου
Βιολογια β λυκείου κεφάλαιο 2
Κεφάλαιο 2 (άνθρωπος και περιβάλλον)
ιστορία α λυκείου κλασσική εποχή
Εξετάστε τις γνώσεις σας στην κλασική εποχή της αρχαίας Ελλάδας, όπως διδάσκεται στην Α' Λυκείου.
ΑΟΘ Κεφάλαιο 2
σημειωσεις κεφαλαιου 2 ΑΟΘ
Βιολογία β Λυκείου
Κεφάλαιο 1 άνθρωπος και υγεία
Κλασική εποχή
Κλασική εποχή: Περίληψη με σημειώσεις
Πληροφορική - Όλη η θεωρία
Περιέχονται όλα τα κομμάτια της ύλης του μαθήματος Πληροφορικής της Γ' Λυκείου
Ολη η θεωρια Αλγεβρας
Ολη η θεωρια Αλγεβρα Α λυκειου, ορισμοι, τυπολογιο, αποδειξεις. Οτι χρειαζεται να διαβασεις για το θεωρητικο κομματι της αλγεβρας.
Δε μπορείς να βρεις αυτό που ψάχνεις; Εξερεύνησε άλλα μαθήματα.
Κριτικές από τους χρήστες μας. Έχουν όλα τα καλά — και το ίδιο θα είχες κι εσύ.
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Χημεία Α’ Λυκείου: Πλήρεις Σημειώσεις
Ετοιμάσου να εξερευνήσεις τον συναρπαστικό κόσμο της χημείας! Σε αυτές τις σημειώσεις θα δεις πώς είναι φτιαγμένη η ύλη γύρω μας, από τα μικροσκοπικά άτομα μέχρι τις περίπλοκες χημικές αντιδράσεις. Οι έννοιες αυτές θα σε βοηθήσουν να καταλάβεις πώς λειτουργεί... Δες περισσότερα

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Το πυρηνικό άτομο
Το άτομο αποτελείται από τον πυρήνα, που περιέχει πρωτόνια (με θετικό φορτίο) και νετρόνια (χωρίς φορτίο). Γύρω από τον πυρήνα περιφέρονται τα ηλεκτρόνια.
Κάθε άτομο χαρακτηρίζεται από δύο βασικούς αριθμούς:
- Ο ατομικός αριθμός (Ζ) δείχνει τον αριθμό των πρωτονίων στον πυρήνα και καθορίζει τη χημική ταυτότητα του στοιχείου
- Ο μαζικός αριθμός (Α) είναι το σύνολο πρωτονίων και νετρονίων στον πυρήνα
Τα ισότοπα είναι άτομα του ίδιου στοιχείου (ίδιο Ζ) αλλά με διαφορετικό αριθμό νετρονίων (διαφορετικό Α). Για παράδειγμα:
- Νάτριο (Na): Z=11, A=23 → 11 πρωτόνια, 12 νετρόνια
- Ασβέστιο (Ca): Z=20, A=40 → 20 πρωτόνια, 20 νετρόνια
Σημαντικό! Το χημικό σύμβολο κάθε στοιχείου γράφεται με το μαζικό αριθμό πάνω αριστερά και τον ατομικό αριθμό κάτω αριστερά π.χ. $^{23}_{11}Na$.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Η μονάδα mol
Το mol είναι η βασική μονάδα ποσότητας ουσίας στο Διεθνές Σύστημα Μονάδων (SI). Ένα mol περιέχει ακριβώς 6,02×10²³ οντότητες (άτομα, μόρια ή ιόντα) - αυτός ο αριθμός ονομάζεται αριθμός Avogadro (N₀).
Ένα mol ατόμων ή μορίων έχει μάζα σε γραμμάρια ίση με την ατομική ή μοριακή μάζα αντίστοιχα. Έτσι:
- 1 mol ατόμων περιέχει N₀ άτομα και ζυγίζει Ar g
- 1 mol μορίων περιέχει N₀ μόρια και ζυγίζει Mr g
Για παράδειγμα, σε ένα μόριο H₂SO₄ υπάρχουν:
- 2 άτομα υδρογόνου (H)
- 1 άτομο θείου (S)
- 4 άτομα οξυγόνου (O)
Αντίστοιχα, σε 1 mol H₂SO₄ έχουμε:
- 2 mol ατόμων H (2N₀ άτομα)
- 1 mol ατόμων S (N₀ άτομα)
- 4 mol ατόμων O (4N₀ άτομα)
Απλοποίηση: Σκέψου το mol ως ένα "πακέτο" ατόμων ή μορίων που περιέχει πάντα τον ίδιο αριθμό σωματιδίων, όπως ένα πακέτο αναψυκτικών περιέχει πάντα 6 κουτάκια.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Μετατροπές μάζας και mol
Η σχέση μεταξύ μάζας (m) μιας ουσίας και του αριθμού mol (n) είναι θεμελιώδης στη χημεία. Χρησιμοποιούμε τη μοριακή μάζα (Mr) για τις μετατροπές αυτές.
Για να βρούμε τον αριθμό mol από τη μάζα: n = m / Mr
Για να βρούμε τη μάζα από τον αριθμό mol: m = n · Mr
Παραδείγματα:
-
Πόσο ζυγίζουν 5 mol νερού (H₂O); Mr(H₂O) = 18 g/mol, άρα m = 5 mol · 18 g/mol = 90 g
-
Πόσο ζυγίζουν 5 mol νατρίου (Na); Mr(Na) = 23 g/mol, άρα m = 5 mol · 23 g/mol = 115 g
-
Πόσο ζυγίζουν 5 mol θειικού οξέος (H₂SO₄); Mr(H₂SO₄) = 98 g/mol, άρα m = 5 mol · 98 g/mol = 490 g
-
Πόσα mol είναι 85 g αμμωνίας (NH₃); Mr(NH₃) = 17 g/mol, άρα n = 85 g / 17 g/mol = 5 mol
Συμβουλή: Σε ασκήσεις χημείας, πάντα ξεκινάμε με τον υπολογισμό της μοριακής μάζας (Mr) των ενώσεων που εμφανίζονται στο πρόβλημα.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Μονάδες συγκέντρωσης διαλυμάτων
Η συγκέντρωση (C) ή molarity (M) ενός διαλύματος δείχνει πόσα mol διαλυμένης ουσίας περιέχονται σε 1 λίτρο (L) διαλύματος:
C = n / V
Από αυτό τον τύπο μπορούμε να υπολογίσουμε:
- Τον αριθμό mol: n = C · V
- Τον όγκο του διαλύματος: V = n / C
- Τη μάζα της διαλυμένης ουσίας: m = n · Mr = C · V · Mr
Παραδείγματα:
-
Πόσα mol H₂SO₄ περιέχονται σε 5L διαλύματος H₂SO₄ 1,9M; n = C · V = 1,9 mol/L · 5L = 9,5 mol
-
Σε πόσα λίτρα διαλύματος H₂SO₄ 1,9M περιέχονται 6 mol H₂SO₄; V = n / C = 6 mol / 1,9 mol/L = 3,15 L
-
Σε 5L διαλύματος H₂SO₄ περιέχονται 588g H₂SO₄. Ποια είναι η συγκέντρωση; Mr(H₂SO₄) = 98 g/mol n = m / Mr = 588g / 98 g/mol = 6 mol C = n / V = 6 mol / 5L = 1,2M
Πρακτική συμβουλή: Στις εξετάσεις, οι ασκήσεις με συγκεντρώσεις απαιτούν προσοχή στις μονάδες. Πάντα μετατρέπουμε τον όγκο σε λίτρα (L) πριν εφαρμόσουμε τους τύπους!

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Αραίωση διαλυμάτων
Κατά την αραίωση ενός διαλύματος, προσθέτουμε διαλύτη (συνήθως νερό) χωρίς να αλλάζει η ποσότητα της διαλυμένης ουσίας. Έτσι, ο αριθμός mol παραμένει σταθερός:
n₁ = n₂ ή C₁·V₁ = C₂·V₂
Όπου:
- C₁, V₁: η αρχική συγκέντρωση και ο αρχικός όγκος
- C₂, V₂: η τελική συγκέντρωση και ο τελικός όγκος
Για παράδειγμα, αν 20mL διαλύματος H₂SO₄ 5M αραιωθούν με προσθήκη 70mL H₂O, η συγκέντρωση του αραιωμένου διαλύματος θα είναι:
- C₁ = 5M
- V₁ = 20mL = 0,020L
- V₂ = V₁ + VH₂O = 20mL + 70mL = 90mL = 0,090L
- C₂ = C₁·V₁/V₂ = 5M·0,020L/0,090L = 1,1M
Ο τύπος C₁·V₁ = C₂·V₂ είναι θεμελιώδης για προβλήματα αραίωσης και χρησιμοποιείται συχνά στο εργαστήριο και στις εξετάσεις.
Θυμήσου: Στην αραίωση ο αριθμός των mol της διαλυμένης ουσίας παραμένει σταθερός, αλλά μοιράζεται σε μεγαλύτερο όγκο, με αποτέλεσμα η συγκέντρωση να μειώνεται.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Διαλυτότητα
Διαλυτότητα είναι η μέγιστη ποσότητα μιας ουσίας που μπορεί να διαλυθεί σε ορισμένη ποσότητα διαλύτη, υπό συγκεκριμένες συνθήκες θερμοκρασίας και πίεσης. Ουσιαστικά, εκφράζει την περιεκτικότητα ενός κορεσμένου διαλύματος.
Τα διαλύματα χαρακτηρίζονται ως:
- Κορεσμένα: περιέχουν τη μέγιστη ποσότητα διαλυμένης ουσίας
- Ακόρεστα: περιέχουν μικρότερη ποσότητα διαλυμένης ουσίας από τη μέγιστη δυνατή
Η διαλυτότητα επηρεάζεται από:
-
Τη φύση του διαλύτη: Ισχύει ο κανόνας "τα όμοια διαλύουν όμοια". Διαλύτης και διαλυμένη ουσία πρέπει να έχουν παρόμοια χημική δομή.
-
Τη θερμοκρασία:
- Για τα στερεά: η διαλυτότητά τους στο νερό αυξάνεται με την αύξηση της θερμοκρασίας
- Για τα αέρια: η διαλυτότητά τους στο νερό μειώνεται με την αύξηση της θερμοκρασίας
-
Την πίεση: Η διαλυτότητα των αερίων στο νερό αυξάνεται με την αύξηση της πίεσης.
Καθημερινή εφαρμογή: Γι' αυτό τα αναψυκτικά χάνουν το ανθρακικό τους (CO₂) όταν ζεσταίνονται ή όταν ανοίγουμε το μπουκάλι (μείωση πίεσης)!

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Ηλεκτρονικές στοιβάδες
Στο ατομικό μοντέλο του Bohr, τα ηλεκτρόνια κινούνται σε καθορισμένες τροχιές (στοιβάδες) γύρω από τον πυρήνα. Κάθε στοιβάδα έχει συγκεκριμένη ενέργεια και χωρητικότητα ηλεκτρονίων.
Για τα γνωστά χημικά στοιχεία υπάρχουν επτά στοιβάδες, που ονομάζονται με τα λατινικά γράμματα K, L, M, N, O, P, Q. Κάθε στοιβάδα χαρακτηρίζεται από τον κύριο κβαντικό αριθμό n.
Η κατανομή των ηλεκτρονίων στις στοιβάδες καθορίζει τις χημικές ιδιότητες του ατόμου. Ιδιαίτερα σημαντικά είναι τα ηλεκτρόνια της εξωτερικής στοιβάδας (ηλεκτρόνια σθένους), που καθορίζουν τη χημική συμπεριφορά του ατόμου.
Η πλήρωση των στοιβάδων γίνεται προοδευτικά από τις εσωτερικές προς τις εξωτερικές, και κάθε στοιβάδα έχει μέγιστη χωρητικότητα 2n² ηλεκτρόνια, όπου n είναι ο κύριος κβαντικός αριθμός.
Χρήσιμο για το σχολείο: Τα στοιχεία με ίδιο αριθμό ηλεκτρονίων στην εξωτερική τους στοιβάδα ανήκουν στην ίδια ομάδα του Περιοδικού Πίνακα και έχουν παρόμοιες χημικές ιδιότητες!

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Περιοδικός Πίνακας Στοιχείων
Ο Περιοδικός Πίνακας οργανώνει τα χημικά στοιχεία με βάση τον ατομικό τους αριθμό (Ζ) σε περιόδους (οριζόντιες σειρές) και ομάδες (κατακόρυφες στήλες).
Μερικά βασικά στοιχεία και οι ιδιότητές τους:
- Υδρογόνο (H): Z=1, περίοδος 1, ομάδα 1Α
- Ήλιο (He): Z=2, περίοδος 1, ομάδα 18Α (ευγενές αέριο)
- Λίθιο (Li): Z=3, περίοδος 2, ομάδα 1Α (αλκάλιο)
- Άνθρακας (C): Z=6, περίοδος 2, ομάδα 14Α
- Οξυγόνο (O): Z=8, περίοδος 2, ομάδα 16Α
- Νάτριο (Na): Z=11, περίοδος 3, ομάδα 1Α (αλκάλιο)
- Χλώριο (Cl): Z=17, περίοδος 3, ομάδα 17Α (αλογόνο)
Τα στοιχεία της ίδιας ομάδας έχουν παρόμοιες ιδιότητες επειδή έχουν τον ίδιο αριθμό ηλεκτρονίων στην εξωτερική τους στοιβάδα. Για παράδειγμα, τα αλκάλια (ομάδα 1Α) έχουν 1 ηλεκτρόνιο στην εξωτερική στοιβάδα και είναι πολύ δραστικά μέταλλα.
Έξυπνο κόλπο: Ο αριθμός της ομάδας (για τις κύριες ομάδες) συχνά αντιστοιχεί στον αριθμό των ηλεκτρονίων της εξωτερικής στοιβάδας!

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Ατομική ακτίνα και περιοδικότητα
Η χημική συμπεριφορά των ατόμων καθορίζεται κυρίως από:
-
Τα ηλεκτρόνια της εξωτερικής στοιβάδας, που συμμετέχουν στους χημικούς δεσμούς.
-
Την ατομική ακτίνα: Όσο μεγαλύτερη είναι η ατομική ακτίνα, τόσο μικρότερη είναι η ελκτική δύναμη του πυρήνα στα εξωτερικά ηλεκτρόνια. Έτσι, τα μεγαλύτερα άτομα αποβάλλουν ευκολότερα ηλεκτρόνια.
Στοιχεία με παρόμοιες χημικές ιδιότητες έχουν παρόμοια ηλεκτρονική δομή στην εξωτερική στοιβάδα. Για παράδειγμα, το Li⁺ και το Na⁺ έχουν παρόμοιες ιδιότητες.
Μεταβολή της ατομικής ακτίνας:
-
Κατά μήκος μιας περιόδου (από αριστερά προς τα δεξιά): Η ατομική ακτίνα μειώνεται, καθώς αυξάνονται τα πρωτόνια και οι ελκτικές δυνάμεις προς τα εξωτερικά ηλεκτρόνια.
-
Κατά μήκος μιας ομάδας (από πάνω προς τα κάτω): Η ατομική ακτίνα αυξάνεται, καθώς αυξάνεται ο αριθμός των στοιβάδων και η απόσταση των εξωτερικών ηλεκτρονίων από τον πυρήνα.
Σημείωση: Όσο μεγαλύτερο είναι ένα άτομο, τόσο πιο αργά κινούνται τα ηλεκτρόνιά του και τόσο ευκολότερα τα αποβάλλει (αν είναι μέταλλο)!

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Περιοδικές ιδιότητες και μεγέθη ατόμων
Η μεταβολή της ατομικής ακτίνας στον περιοδικό πίνακα ακολουθεί συγκεκριμένα μοτίβα που μας βοηθούν να κατανοήσουμε και να προβλέψουμε τη χημική συμπεριφορά των στοιχείων.
Κατά μήκος μιας περιόδου (από αριστερά προς τα δεξιά):
- Η ατομική ακτίνα μειώνεται
- Ο ατομικός αριθμός αυξάνεται, προσθέτοντας πρωτόνια στον πυρήνα
- Η ελκτική δύναμη του πυρήνα προς τα ηλεκτρόνια σθένους αυξάνεται
- Τα ηλεκτρόνια έλκονται πιο κοντά στον πυρήνα, μειώνοντας το μέγεθος του ατόμου
Κατά μήκος μιας ομάδας (από πάνω προς τα κάτω):
- Η ατομική ακτίνα αυξάνεται
- Ο αριθμός των ηλεκτρονικών στοιβάδων αυξάνεται
- Η απόσταση της εξωτερικής στοιβάδας από τον πυρήνα μεγαλώνει
- Η ελκτική δύναμη του πυρήνα μειώνεται λόγω της απόστασης
- Το άτομο γίνεται μεγαλύτερο
Πρακτική σημασία: Αυτή η γνώση μας βοηθά να προβλέψουμε τη δραστικότητα των μετάλλων. Για παράδειγμα, το κάλιο (K) είναι πιο δραστικό από το νάτριο (Na) επειδή έχει μεγαλύτερη ατομική ακτίνα και αποβάλλει ευκολότερα το εξωτερικό του ηλεκτρόνιο.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Νομίζαμε ότι δε θα ρωτούσες ποτέ...
Τι είναι ο AI σύντροφος του Knowunity;
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Πού μπορώ να κατεβάσω την εφαρμογή Knowunity;
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Πώς μπορώ να λάβω την πληρωμή μου; Πόσα μπορώ να κερδίσω;
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
Πιο δημοφιλή περιεχόμενα στο Χημεία
9Οργανική χημεία
Όλες οι αντιδράσεις ανά κατηγορία.
Ονοματολογία κυριων στοιχείων
Χημεια α λυκειου
χημεια γ λυκειου
Έλεγχος γνώσεων στην χημεία της Γ' Λυκείου. Εξετάζονται θέματα οργανικής χημείας, αντιδράσεων και ενώσεων.
Ονοματολογία
Χημεία Α λυκείου
Χημεία α λυκείου
1ο ,2ο ,3ο κεφάλαιο χημείας α λυκείου
χημική ισορροπία
όλο το κεφάλαιο
χημική κινητική
όλες οι σημειώσεις του κεφαλαίου
Διαμοριακές δυνάμεις Χημεία Γ' λυκείου
Σημειωσεις στο κεφάλαιο των διαμοριακών δυνάμεων της χημειας γ λυκειου
Θερμοχημεία - Ενθαλπία
Επεξήγηση, περιληπτική, του κεφαλαίου της Θερμοχημειας στην ύλη της Γ´ Λυκείου.
Πιο δημοφιλή περιεχόμενα
9Ιστορια β λυκειου ολοι οι ορισμοι τις τραπεζας
Ορισμοί ιστόριας
Σχεδιαγράμματα όλης της ύλης ιστορίας α λυκείου
Σας έχω σχεδιαγράμματα όλης της εξεταστέας ύλης της α λυκείου για να διευκολυνθείτε από το τεράστιο βάρος του βιβλίου
Βιολογια β λυκείου κεφάλαιο 2
Κεφάλαιο 2 (άνθρωπος και περιβάλλον)
ιστορία α λυκείου κλασσική εποχή
Εξετάστε τις γνώσεις σας στην κλασική εποχή της αρχαίας Ελλάδας, όπως διδάσκεται στην Α' Λυκείου.
ΑΟΘ Κεφάλαιο 2
σημειωσεις κεφαλαιου 2 ΑΟΘ
Βιολογία β Λυκείου
Κεφάλαιο 1 άνθρωπος και υγεία
Κλασική εποχή
Κλασική εποχή: Περίληψη με σημειώσεις
Πληροφορική - Όλη η θεωρία
Περιέχονται όλα τα κομμάτια της ύλης του μαθήματος Πληροφορικής της Γ' Λυκείου
Ολη η θεωρια Αλγεβρας
Ολη η θεωρια Αλγεβρα Α λυκειου, ορισμοι, τυπολογιο, αποδειξεις. Οτι χρειαζεται να διαβασεις για το θεωρητικο κομματι της αλγεβρας.
Δε μπορείς να βρεις αυτό που ψάχνεις; Εξερεύνησε άλλα μαθήματα.
Κριτικές από τους χρήστες μας. Έχουν όλα τα καλά — και το ίδιο θα είχες κι εσύ.
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.