¿Alguna vez te has preguntado por qué algunos elementos reaccionan... Δες περισσότερα
Tendencias y Propiedades en la Tabla Periódica






Introducción a las Propiedades Periódicas
Las propiedades periódicas son las características de los elementos que varían de forma predecible en la tabla periódica. Esta periodicidad se debe a cómo se repiten las configuraciones electrónicas de la capa de valencia.
Hay dos conceptos clave que explican todo: la carga nuclear efectiva es la carga positiva "real" que siente un electrón de valencia. No es igual al número atómico porque los electrones internos "apantallan" parte de esa carga.
En un periodo (→): Z_ef aumenta porque hay más protones pero los electrones van a la misma capa. En un grupo (↓): Z_ef se mantiene casi constante para la última capa porque aunque hay más protones, también hay más capas internas que apantallan.
¡Dato clave! El efecto pantalla es como un escudo: los electrones internos protegen a los de valencia de la atracción total del núcleo.

Radio Atómico
El radio atómico es la mitad de la distancia entre núcleos de dos átomos idénticos enlazados. Es como medir el "tamaño" de un átomo.
En un grupo (↓): aumenta porque se añaden nuevas capas electrónicas. Cada capa nueva está más lejos del núcleo, así que el átomo es más grande. En un periodo (→): disminuye porque aunque el número de capas es el mismo, la Z_ef aumenta y "tira" más fuerte de los electrones, contrayendo el átomo.
Piénsalo así: es como si el núcleo fuera un imán que se hace más fuerte hacia la derecha (mismo periodo) pero más débil hacia abajo (mismo grupo) debido a la distancia.
Truco para recordar: Los átomos más grandes están en la esquina inferior izquierda, los más pequeños en la superior derecha.

Radio Iónico
Cuando un átomo gana o pierde electrones, su tamaño cambia drásticamente. Los cationes (iones positivos) son más pequeños que el átomo neutro porque al perder electrones, a menudo se pierde toda la capa de valencia y los restantes son atraídos con más fuerza.
Los aniones (iones negativos) son más grandes que el átomo neutro. Al ganar electrones en la misma capa, aumenta la repulsión entre ellos y la nube electrónica se expande.
Para especies isoelectrónicas (mismo número de electrones), a más protones en el núcleo, menor radio. Es lógico: más "tirón" hacia el centro.
Regla fácil: Perder electrones = encogerse, ganar electrones = hincharse.

Energía de Ionización
La energía de ionización (EI) es la energía necesaria para "arrancar" un electrón de un átomo gaseoso. Es como la fuerza que necesitas para separar algo que está pegado.
En un grupo (↓): disminuye porque los electrones están más lejos y más apantallados. En un periodo (→): aumenta porque la Z_ef aumenta y los electrones están más "pegados" al núcleo.
¡Cuidado con las excepciones! Grupo 2 vs. 13: El grupo 13 tiene EI menor porque es más fácil quitar un electrón p que uno de un orbital s completo. Grupo 15 vs. 16: El grupo 16 tiene EI menor porque elimina la repulsión de electrones emparejados.
Para examen: Aprende las excepciones de memoria. Be > B y N > O son preguntas típicas.

Afinidad Electrónica y Electronegatividad
La afinidad electrónica (AE) mide cuánto "le gusta" a un átomo aceptar un electrón. Si es muy negativa, significa que libera mucha energía al aceptarlo (es favorable).
En un grupo (↓): menos negativa (menos favorable) porque el electrón entrante está más lejos del núcleo. En un periodo (→): más negativa (más favorable) porque la Z_ef aumenta.
La electronegatividad es la capacidad de atraer electrones en un enlace. El flúor es el más electronegativo (4.0 en la escala de Pauling). Sigue las mismas tendencias: aumenta hacia la derecha y hacia arriba.
Dato importante: Los gases nobles tienen AE positiva - ¡no quieren electrones extra!
Ejemplos y Casos Prácticos
Para ordenar por radio atómico creciente: P, Cl, Na, Al (todos del periodo 3), aplicamos que el radio disminuye hacia la derecha. Resultado: Cl < P < Al < Na.
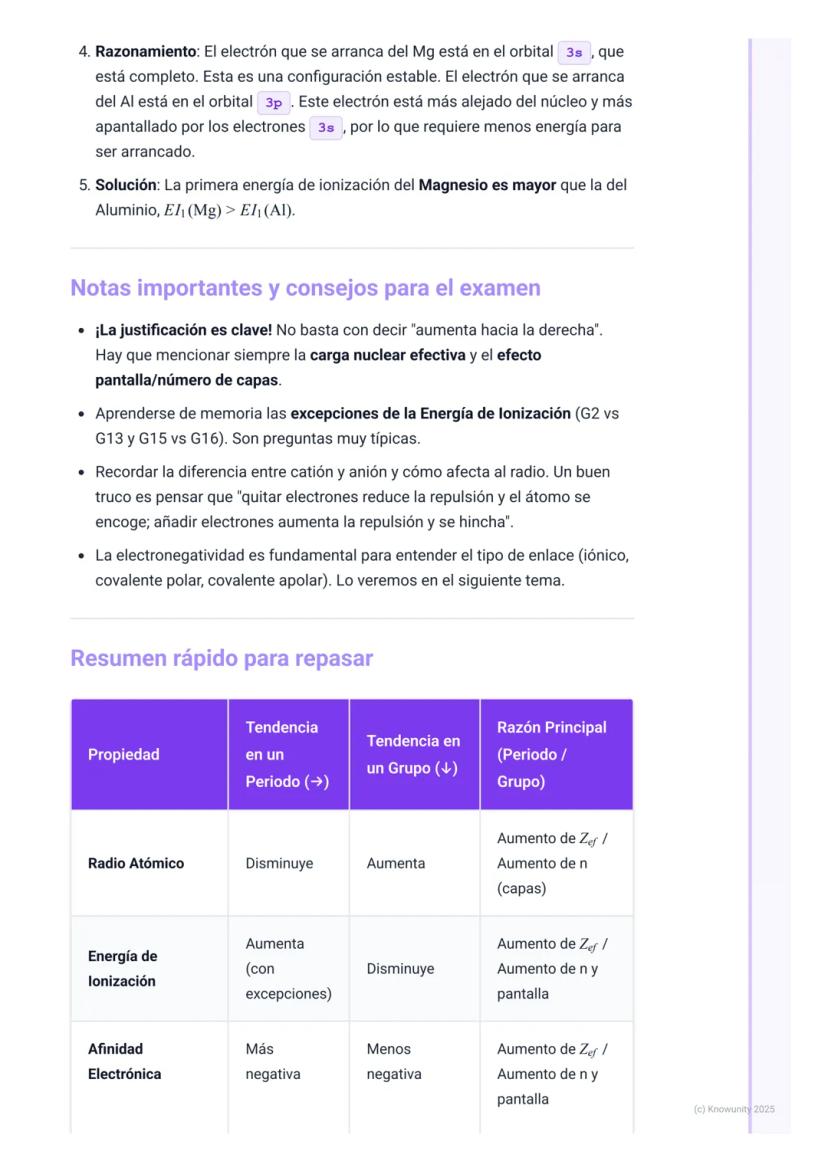
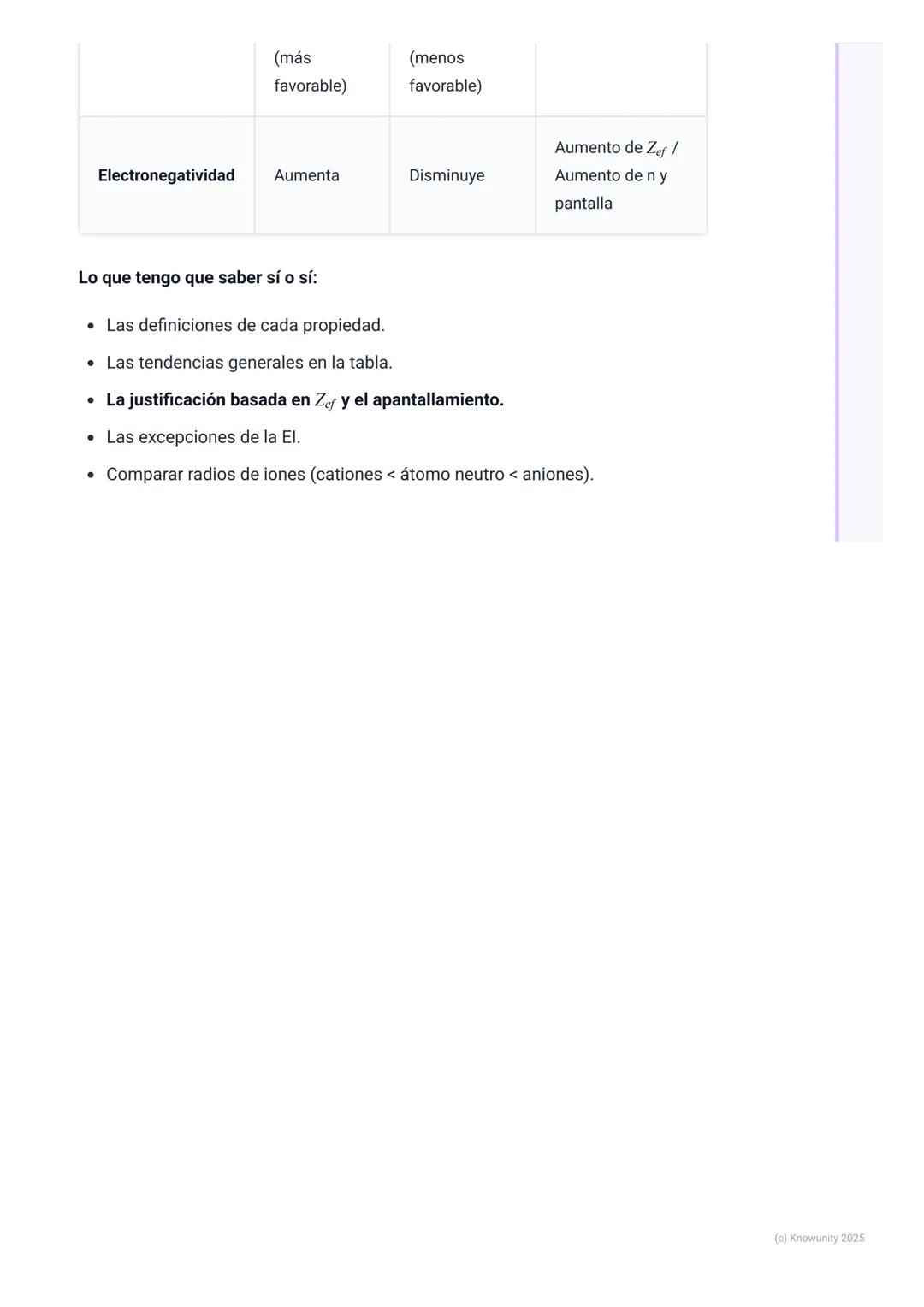
Para comparar energías de ionización entre Mg y Al, aunque Al está más a la derecha, EI(Mg) > EI(Al) por la excepción del grupo 2 vs. 13. El electrón 3p del Al es más fácil de arrancar que el 3s del Mg.
Las especies isoelectrónicas como O²⁻, F⁻, Ne, Na⁺, Mg²⁺ se ordenan por número de protones: a más protones, menor radio.
Clave del éxito: En el examen, siempre justifica con Z_ef y apantallamiento, no solo digas "aumenta hacia la derecha".
Resumen para Repasar
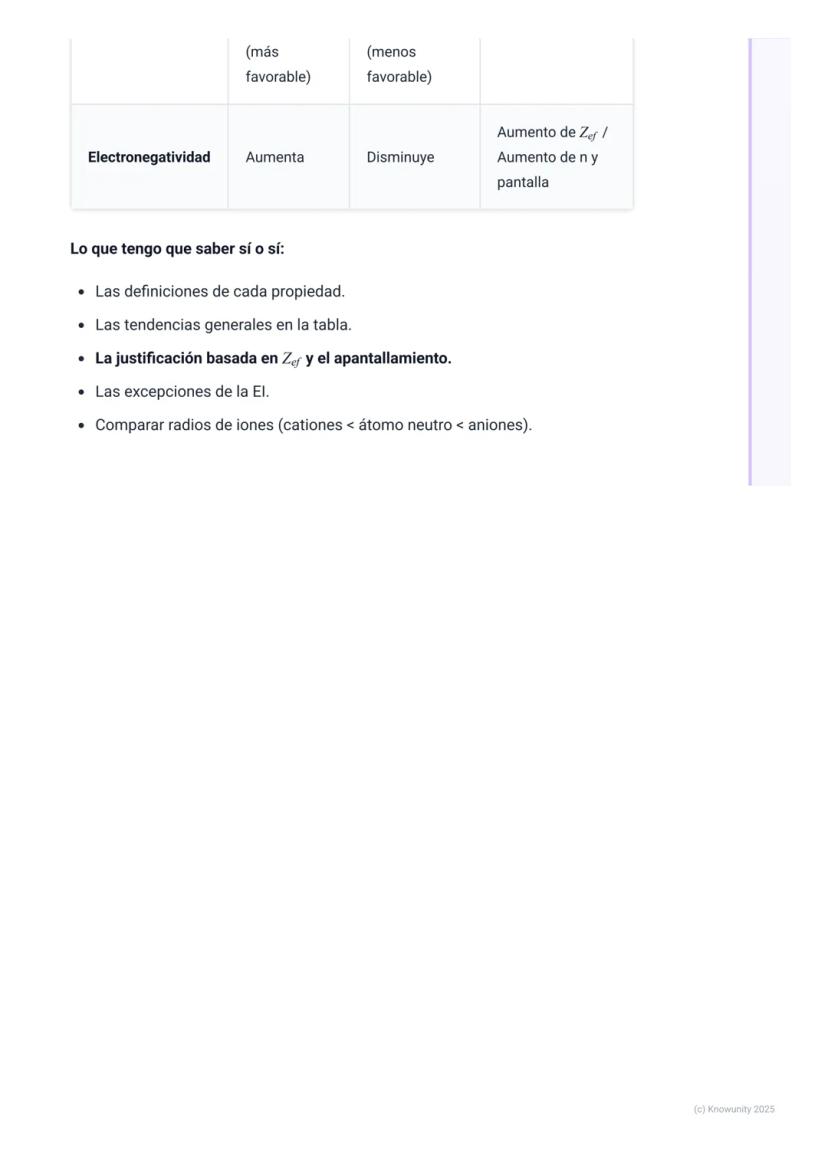
| Propiedad | Periodo (→) | Grupo (↓) | Razón |
|---|---|---|---|
| **Radio atómico** | Disminuye | Aumenta | Z_ef vs. capas nuevas |
| **Energía ionización** | Aumenta* | Disminuye | Z_ef vs. distancia+pantalla |
| **Afinidad electrónica** | Más negativa | Menos negativa | Z_ef vs. distancia+pantalla |
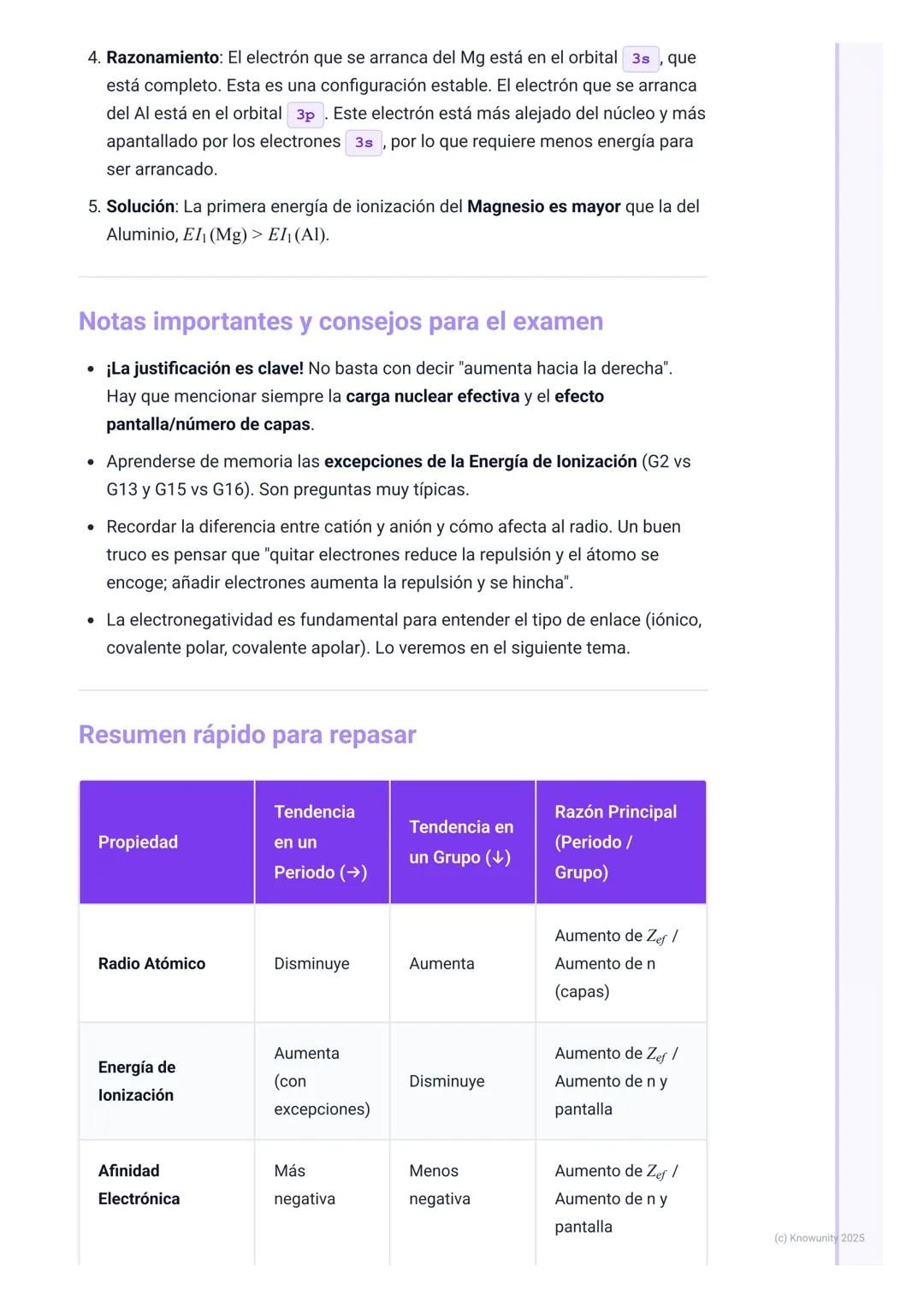
| **Electronegatividad** | Aumenta | Disminuye | Z_ef vs. distancia+pantalla |
*Con excepciones importantes
Lo esencial para el examen: definiciones, tendencias generales, justificaciones con Z_ef, excepciones de EI (G2 vs G13, G15 vs G16), y comparación de radios iónicos.
Consejo final: Practica con ejemplos hasta que puedas predecir propiedades sin mirar la tabla. ¡Es como tener superpoderes químicos!
Νομίζαμε ότι δε θα ρωτούσες ποτέ...
Τι είναι ο AI σύντροφος του Knowunity;
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Πού μπορώ να κατεβάσω την εφαρμογή Knowunity;
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Πώς μπορώ να λάβω την πληρωμή μου; Πόσα μπορώ να κερδίσω;
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
Πιο δημοφιλή περιεχόμενα στο Química
9Ácido - Base
Aquí os dejo unos resúmenes completos con puntos claves y explicaciones de este tema. Realizados por mi en GoodNotes.
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Reacciones ácido-base
Apuntes de reacciones ácido-base de segundo de bachillerato
Termoquímica
Apuntes de termoquímica y algunos ejercicios para 2Bach
Equilibrio Químico Resumen
Resumen de elquilibro químico de 2º de bachillerato
Reacciones de transferencia de electrones. Oxidación - reducción
Apuntes de REDOX de química de 2° de bachillerato
ESQUEMA REDOX
Reacciones óxido reducción de química Preguntan mucho en EBAU
Equilibrio químico y solubilidad
Apuntes de equilibrio químico y solubilidad de química de 2° de bachillerato
Química orgánica
basicas de la química orgánica
Πιο δημοφιλή περιεχόμενα
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
Δε μπορείς να βρεις αυτό που ψάχνεις; Εξερεύνησε άλλα μαθήματα.
Κριτικές από τους χρήστες μας. Έχουν όλα τα καλά — και το ίδιο θα είχες κι εσύ.
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.
Tendencias y Propiedades en la Tabla Periódica
¿Alguna vez te has preguntado por qué algunos elementos reaccionan violentamente y otros apenas lo hacen? La respuesta está en las propiedades periódicas, esas características que cambian de manera predecible a lo largo de la tabla periódica. Dominar estas tendencias... Δες περισσότερα

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Introducción a las Propiedades Periódicas
Las propiedades periódicas son las características de los elementos que varían de forma predecible en la tabla periódica. Esta periodicidad se debe a cómo se repiten las configuraciones electrónicas de la capa de valencia.
Hay dos conceptos clave que explican todo: la carga nuclear efectiva es la carga positiva "real" que siente un electrón de valencia. No es igual al número atómico porque los electrones internos "apantallan" parte de esa carga.
En un periodo (→): Z_ef aumenta porque hay más protones pero los electrones van a la misma capa. En un grupo (↓): Z_ef se mantiene casi constante para la última capa porque aunque hay más protones, también hay más capas internas que apantallan.
¡Dato clave! El efecto pantalla es como un escudo: los electrones internos protegen a los de valencia de la atracción total del núcleo.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Radio Atómico
El radio atómico es la mitad de la distancia entre núcleos de dos átomos idénticos enlazados. Es como medir el "tamaño" de un átomo.
En un grupo (↓): aumenta porque se añaden nuevas capas electrónicas. Cada capa nueva está más lejos del núcleo, así que el átomo es más grande. En un periodo (→): disminuye porque aunque el número de capas es el mismo, la Z_ef aumenta y "tira" más fuerte de los electrones, contrayendo el átomo.
Piénsalo así: es como si el núcleo fuera un imán que se hace más fuerte hacia la derecha (mismo periodo) pero más débil hacia abajo (mismo grupo) debido a la distancia.
Truco para recordar: Los átomos más grandes están en la esquina inferior izquierda, los más pequeños en la superior derecha.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Radio Iónico
Cuando un átomo gana o pierde electrones, su tamaño cambia drásticamente. Los cationes (iones positivos) son más pequeños que el átomo neutro porque al perder electrones, a menudo se pierde toda la capa de valencia y los restantes son atraídos con más fuerza.
Los aniones (iones negativos) son más grandes que el átomo neutro. Al ganar electrones en la misma capa, aumenta la repulsión entre ellos y la nube electrónica se expande.
Para especies isoelectrónicas (mismo número de electrones), a más protones en el núcleo, menor radio. Es lógico: más "tirón" hacia el centro.
Regla fácil: Perder electrones = encogerse, ganar electrones = hincharse.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Energía de Ionización
La energía de ionización (EI) es la energía necesaria para "arrancar" un electrón de un átomo gaseoso. Es como la fuerza que necesitas para separar algo que está pegado.
En un grupo (↓): disminuye porque los electrones están más lejos y más apantallados. En un periodo (→): aumenta porque la Z_ef aumenta y los electrones están más "pegados" al núcleo.
¡Cuidado con las excepciones! Grupo 2 vs. 13: El grupo 13 tiene EI menor porque es más fácil quitar un electrón p que uno de un orbital s completo. Grupo 15 vs. 16: El grupo 16 tiene EI menor porque elimina la repulsión de electrones emparejados.
Para examen: Aprende las excepciones de memoria. Be > B y N > O son preguntas típicas.

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Afinidad Electrónica y Electronegatividad
La afinidad electrónica (AE) mide cuánto "le gusta" a un átomo aceptar un electrón. Si es muy negativa, significa que libera mucha energía al aceptarlo (es favorable).
En un grupo (↓): menos negativa (menos favorable) porque el electrón entrante está más lejos del núcleo. En un periodo (→): más negativa (más favorable) porque la Z_ef aumenta.
La electronegatividad es la capacidad de atraer electrones en un enlace. El flúor es el más electronegativo (4.0 en la escala de Pauling). Sigue las mismas tendencias: aumenta hacia la derecha y hacia arriba.
Dato importante: Los gases nobles tienen AE positiva - ¡no quieren electrones extra!

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Ejemplos y Casos Prácticos
Para ordenar por radio atómico creciente: P, Cl, Na, Al (todos del periodo 3), aplicamos que el radio disminuye hacia la derecha. Resultado: Cl < P < Al < Na.
Para comparar energías de ionización entre Mg y Al, aunque Al está más a la derecha, EI(Mg) > EI(Al) por la excepción del grupo 2 vs. 13. El electrón 3p del Al es más fácil de arrancar que el 3s del Mg.
Las especies isoelectrónicas como O²⁻, F⁻, Ne, Na⁺, Mg²⁺ se ordenan por número de protones: a más protones, menor radio.
Clave del éxito: En el examen, siempre justifica con Z_ef y apantallamiento, no solo digas "aumenta hacia la derecha".

Κάνε εγγραφή για να δεις το ΠΕΡΙΕΧΟΜΕΝΟ. Είναι δωρεάν!
- Πρόσβαση σε όλα τα έγγραφα
- Βελτίωσε τους βαθμούς σου
- Γίνε μέλος με εκατομμύρια μαθητές
Resumen para Repasar
| Propiedad | Periodo (→) | Grupo (↓) | Razón |
|---|---|---|---|
| **Radio atómico** | Disminuye | Aumenta | Z_ef vs. capas nuevas |
| **Energía ionización** | Aumenta* | Disminuye | Z_ef vs. distancia+pantalla |
| **Afinidad electrónica** | Más negativa | Menos negativa | Z_ef vs. distancia+pantalla |
| **Electronegatividad** | Aumenta | Disminuye | Z_ef vs. distancia+pantalla |
*Con excepciones importantes
Lo esencial para el examen: definiciones, tendencias generales, justificaciones con Z_ef, excepciones de EI (G2 vs G13, G15 vs G16), y comparación de radios iónicos.
Consejo final: Practica con ejemplos hasta que puedas predecir propiedades sin mirar la tabla. ¡Es como tener superpoderes químicos!
Νομίζαμε ότι δε θα ρωτούσες ποτέ...
Τι είναι ο AI σύντροφος του Knowunity;
Ο AI σύντροφός μας είναι ειδικά σχεδιασμένος για τις ανάγκες των μαθητών. Βασισμένοι στα εκατομμύρια κομμάτια Περιεχομένων που έχουμε στην πλατφόρμα, μπορούμε να παρέχουμε πραγματικά ουσιαστικές και σχετικές απαντήσεις στους μαθητές. Αλλά δεν αφορά μόνο τις απαντήσεις, ο σύντροφος είναι ακόμη περισσότερο για την καθοδήγηση των μαθητών στις καθημερινές τους μαθησιακές προκλήσεις, με εξατομικευμένα προγράμματα μελέτης, κουίζ ή Περιεχόμενα στη Συνομιλία και 100% εξατομίκευση βασισμένη στις δεξιότητες και την ανάπτυξη των μαθητών.
Πού μπορώ να κατεβάσω την εφαρμογή Knowunity;
Μπορείτε να κατεβάσετε την εφαρμογή από το Google Play Store και το Apple App Store.
Πώς μπορώ να λάβω την πληρωμή μου; Πόσα μπορώ να κερδίσω;
Ναι, έχετε δωρεάν πρόσβαση στο περιεχόμενο της εφαρμογής και στον AI companion μας. Για να ξεκλειδώσετε ορισμένες λειτουργίες της εφαρμογής, μπορείτε να αγοράσετε το Knowunity Pro.
Πιο δημοφιλή περιεχόμενα στο Química
9Ácido - Base
Aquí os dejo unos resúmenes completos con puntos claves y explicaciones de este tema. Realizados por mi en GoodNotes.
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Reacciones ácido-base
Apuntes de reacciones ácido-base de segundo de bachillerato
Termoquímica
Apuntes de termoquímica y algunos ejercicios para 2Bach
Equilibrio Químico Resumen
Resumen de elquilibro químico de 2º de bachillerato
Reacciones de transferencia de electrones. Oxidación - reducción
Apuntes de REDOX de química de 2° de bachillerato
ESQUEMA REDOX
Reacciones óxido reducción de química Preguntan mucho en EBAU
Equilibrio químico y solubilidad
Apuntes de equilibrio químico y solubilidad de química de 2° de bachillerato
Química orgánica
basicas de la química orgánica
Πιο δημοφιλή περιεχόμενα
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
Δε μπορείς να βρεις αυτό που ψάχνεις; Εξερεύνησε άλλα μαθήματα.
Κριτικές από τους χρήστες μας. Έχουν όλα τα καλά — και το ίδιο θα είχες κι εσύ.
Η εφαρμογή είναι πολύ εύκολη στη χρήση και καλά σχεδιασμένη. Έχω βρει ό,τι έψαχνα μέχρι τώρα και έχω μάθει πολλά από τις παρουσιάσεις! Σίγουρα θα χρησιμοποιήσω την εφαρμογή για μια εργασία του μαθήματος! Και φυσικά βοηθάει πολύ και ως έμπνευση.
Αυτή η εφαρμογή είναι πραγματικά τέλεια. Υπάρχουν τόσες πολλές σημειώσεις μελέτης και βοήθεια [...]. Το μάθημα που με δυσκολεύει είναι τα Γαλλικά, για παράδειγμα, και η εφαρμογή έχει τόσες επιλογές για βοήθεια. Χάρη σε αυτή την εφαρμογή, έχω βελτιώσει τα Γαλλικά μου. Θα την πρότεινα σε οποιονδήποτε.
Ουάου, είμαι πραγματικά εντυπωσιασμένος. Δοκίμασα την εφαρμογή επειδή την είδα διαφημισμένη πολλές φορές και έμεινα άφωνος. Αυτή η εφαρμογή είναι Η ΒΟΗΘΕΙΑ που χρειάζεσαι για το σχολείο και πάνω απ' όλα, προσφέρει τόσα πράγματα, όπως ασκήσεις και φύλλα γεγονότων, που ήταν ΠΟΛΥ χρήσιμα για μένα προσωπικά.